Nat Commun:化疗或会改变胰腺癌患者机体的免疫细胞“蓝图” |
 |
来源:100医药网原创 2023-03-30 09:57
来自美国纽约大学朗格尼健康中心等机构的科学家们通过研究发现,化疗或会影响患者机体免疫系统攻击胰腺肿瘤的能力。胰腺导管腺癌的肿瘤微环境是一种能驱动肿瘤进展的复杂生态系统,然而,目前研究人员并不清楚胰腺导管腺癌肿瘤微环境中的深入单细胞特征以及其在对疗法反应中所扮演的关键角色。近日,一篇发表在国际杂志Nature Communications上题为 Single-cell RNA sequencing reveals the effects of chemotherapy on human pancreatic adenocarcinoma and its tumor microenvironment 的研究报告中,来自美国纽约大学朗格尼健康中心等机构的科学家们通过研究发现,化疗或会影响患者机体系统攻击胰腺肿瘤的能力。
研究者表示,这项研究主要围绕着宿主机体的免疫系统而开展,其中就包括能攻击诸如病毒等外源性有机体的T细胞,为了保护正常细胞,免疫系统会利用T细胞表面诸如PD1等检查点分子来在其收到正确信号时关闭T细胞的攻击。机体往往能识别出肿瘤的异常,但癌细胞会拦截检查点从而关闭机体的免疫反应,一种非常突出的免疫疗法就能试图关闭检查点,从而使得癌细胞对免疫系统再次可见。
这项研究中,研究人员收集并分析了来自27名胰腺导管腺癌患者机体中超过13.9万份肿瘤细胞,其中仅有12%的患者在后存活超过了5年时间;据研究者介绍,对肿瘤组织周围强烈的免疫反应是缩小胰腺中这些肿瘤的关键。当研究人员对11名患者在化疗前和化疗后6个月时进行比较,结果发现,治疗后患者机体中特定抑制性检查点分子的产量下降了3倍,阻断这些信号,尤其是PD1是当前设计的抵御很多癌症的免疫疗法的目标,但迄今为止其证明对胰腺导管腺癌是无效的。重要的是,研究者发现名为TIGIT的第二个检查点或许是胰腺导管腺癌中最常见的抑制性检查点分子,在化疗进行前相比PD1而言其可用作治疗性靶点的概率是前者的18倍,但在化疗后却仅为5倍了。这些研究发现或许值得进一步分析从而阐明是否基于TIGIT的免疫疗法能比靶向作用PD1(即程序性细胞死亡蛋白1)的免疫疗法更能有效治疗胰腺导管腺癌。
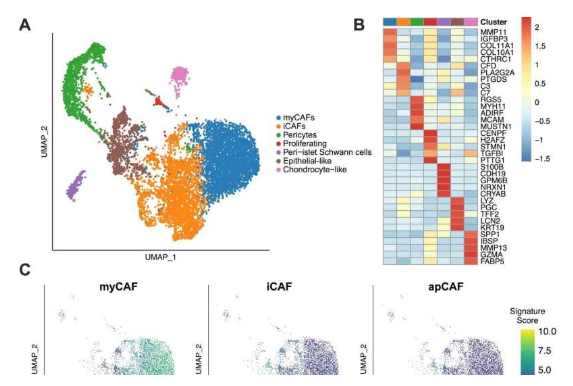
化疗或会改变患者机体的免疫细胞 蓝图 。
图片来源:Nature Communications (2023). DOI:10.1038/s41467-023-36296-4
研究者Aristotelis Tsirigos,说道,本文研究结果揭示了化疗如何对胰腺导管腺癌中肿瘤微环境的细胞蓝图产生深远的影响。重要的是,化疗会促进胰腺导管腺癌对后续免疫疗法的耐受性。研究者补充道,后期他们还需要进一步研究来确定是否由于潜在的耐受性,在治疗时化疗就需要与免疫疗法组合使用来治疗顽固且致命性的癌症形式。化疗后的其它改变往往会体现在其它免疫细胞数量、细胞之间互动的机制、以及其它癌症相关免疫细胞(比如成纤维细胞和巨噬细胞)的减少,这些细胞如果不加以控制对话就会促进癌症生长,然而研究者认为,这些分子改变对疗法产生的确切影响还有待于进一步研究确定。
研究者Tsirigos说道,目前他们正在进行更多的额外试验来在更多患者中证实这些研究结果,后期或许还需要进一步深入研究来评估是否通过名为scRNA-seq技术对确诊后不久的患者机体的肿瘤微环境进行详细的细胞分析就能帮助制定未来的疗法决策。随着新技术能让研究人员在细胞水平上观察患者机体中发生了什么,于是研究人员就会开始调整对免疫疗法的评估,并可能根据肿瘤周围实际发生的情况来决定如何最好地使用它们,综上,本文研究结果表明,化疗或许会对胰腺导管腺癌的肿瘤微环境产生深远的影响并可能会促进癌症对免疫疗法的耐受性。(100yiyao.com)
原始出处:
Werba, G., Weissinger, D., Kawaler, E.A.et al..Nat Commun14, 797 (2023). doi:10.1038/s41467-023-36296-4
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 第三轮通知 | 2025年CSEV第九届细胞外囊泡大会倒计时2天! (2025-10-22)
- Adv Sci/eLife:中山大学高国全/杨霞/齐炜炜团队从代谢角度揭示阿尔兹海默症认知功能障碍的新调控分子 (2025-10-22)
- 《自然·代谢》:巨噬细胞竟是个“醋坛子”!中科院/复旦团队首次发现,肝癌用乳酸诱导巨噬细胞合成乙酸,促进自身转移 (2025-10-22)
- 上海德达心血管医院成功举办《胸痛的识别和心脏大血管疾病的规范治疗》研讨会 (2025-10-22)
- 第八届(2025)中国医疗器械创新创业大赛人工智能与医用机器人类别赛圆满落幕 (2025-10-21)
- 《肝病学》:世界首例活体异种肝移植!基因改造猪肝体内存续38天,患者存活171天 (2025-10-21)
- 《癌症研究》:手术促癌转移证据+1!科学家发现,手术会导致中性粒细胞胞外陷阱形成,重编程癌细胞代谢,促进癌细胞存活和转移 (2025-10-21)
- Nature Genetics:变“在场”为“在岗”——基于剪接修复的活性筛选系统,重塑高分辨率碱基编辑扫描新范式 (2025-10-21)
- 儿童营养不良后增重别盲目!Matern Child Nutr:男性康复期快速增重,成年肥胖风险显著升高 (2025-10-20)
- 《自然》杂志刊文:首次揭示决定胰腺癌细胞命运的关键调控因子 (2025-10-20)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















