CRM:乳酸终于出卖了肿瘤!科学家发明新型给药系统,专打产生乳酸的肿瘤 |
 |
来源:奇点糕 2025-01-30 15:02
该乳酸响应给药系统,利用肿瘤产生乳酸这一特征,大幅提升了药物对肿瘤的靶向性和治疗效果。肿瘤通过有氧糖酵解(瓦博格效应)产生的乳酸,简直是恶贯满盈。
我们曾经介绍过,乳酸可以将瘤内的巨噬细胞从抗癌型变成促癌型[1-3],可以增强调节性T细胞的抑制功能[4],还能把PD-1抑制剂变成促进免疫抑制的 毒药 [5]。
去年4月份,苏州大学团队还发现乳酸会导致抑癌蛋白p53乳酸化,失去抗癌功能[6];同年7月,中山大学团队又发现,乳酸会促进修复DNA损伤,帮助癌细胞抵抗[7]。
乳酸给肿瘤带去那么多好处,难道我们就没有办法治它了么?
近日,由芝加哥大学吴小阳/Huang Jun领衔的研究团队,在著名期刊Cell Reports Medicine上发表一篇重要研究论文[8],创新性发明了一种乳酸特异性给药系统,专门针对爱产乳酸的肿瘤。采用这个给药系统之后,可以大幅提高的肿瘤组织特异性和疗效。

▲论文首页截图
与健康组织相比,肿瘤组织的代谢发生了重编程。有氧糖酵解或瓦博格效应,是癌细胞的共同特征。
这种代谢的变化会促使肿瘤产生大量的乳酸,导致肿瘤微环境乳酸浓度(10-40mM)升高到健康组织(1mM)的十到数十倍。
大量的乳酸聚集会导致肿瘤组织的pH值降低,虽然当前已经存在pH值响应型给药系统,但是这些系统往往需要强酸环境,而肿瘤微环境还达不到;另外,pH也不具有肿瘤特异性。
为了解决上述难题,吴小阳团队开发了一款乳酸响应给药系统 酶辅助Janus介孔二氧化硅纳米颗粒。这个给药系统中包含了特异性识别乳酸的乳酸氧化酶,乳酸氧化酶会把乳酸分解成丙酮酸和过氧化氢,过氧化氢可以作用于给药系统,导致药物的释放。
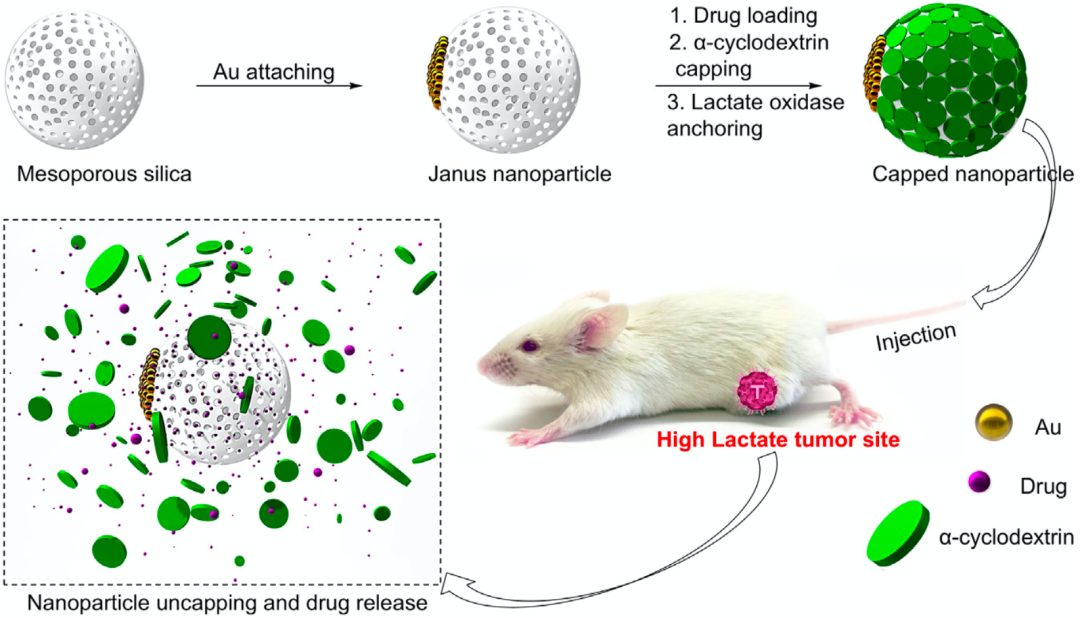
▲乳酸响应给药系统示意图
有了上面的给药系统之后,就要测试它的载药和给药能力了。吴小阳团队选择的抗癌药物,是自带荧光的常用化疗药。
通过给药小鼠一个小时之后,就可在肿瘤和一些器官中检测到荧光信号。吴小阳团队还注意到,与直接注射多柔比星或pH响应系统相比,注射乳酸响应系统的小鼠,多柔比星在肿瘤中的分布有特异性增加,而在其他健康器官(包括心脏、肝脏、肌肉和肾脏)中的分布则没有增加。
从下图可以直观地看出,乳酸响应系统具有肿瘤特异性,而且往肿瘤内给药的效率非常高,瘤内抗癌药峰值浓度可增加10倍左右。
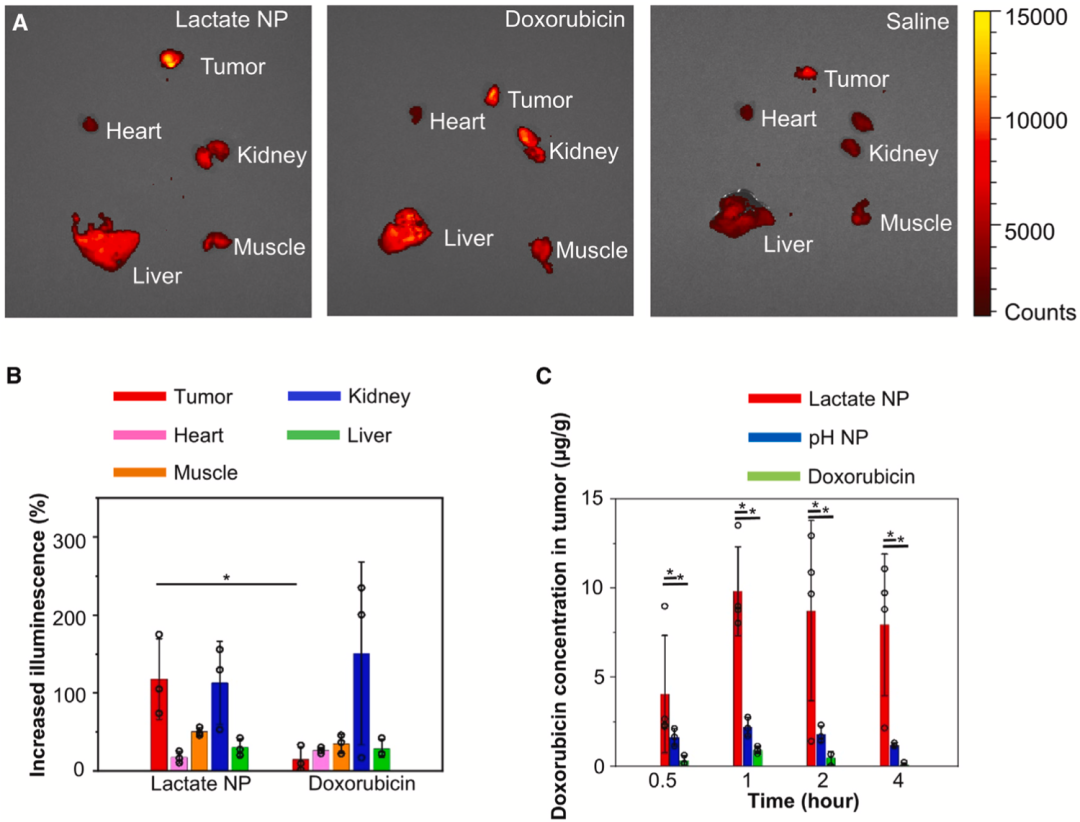
▲不同给药方式的比较
基于4T1细胞系的荷瘤小鼠研究显示,乳酸响应给药系统治疗的小鼠肿瘤体积显著缩小,生存时间显著延长。
值得一提的是,即使是对于已经发生肺转移的乳腺癌小鼠模型,乳酸响应给药系统也能抑制转移灶的生长,并延长小鼠存活时间。
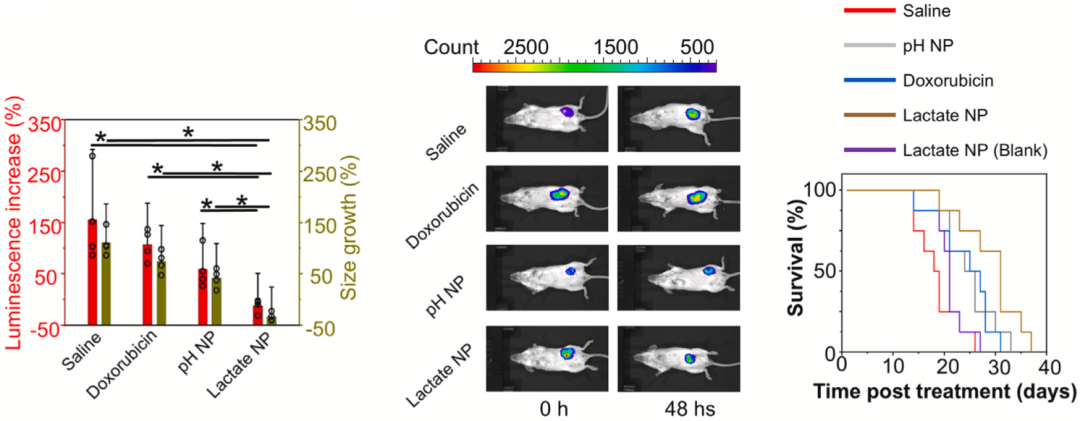
▲乳酸响应给药系统的抗肿瘤效果
除了化疗药物多柔比星之外,吴小阳团队还测试了用乳酸响应给药系统搭载小分子STING激动剂SR-717的抗癌效果。
从研究结果来看,这种给药方式也能提升免疫治疗药物SR-717的抗癌效果。此外,他们还测试了搭载SR-717的乳酸响应给药系统联合PD-1抑制剂的治疗效果。从下图曲线可以看出,与其他疗法相比,联合治疗的疗效非常突出。
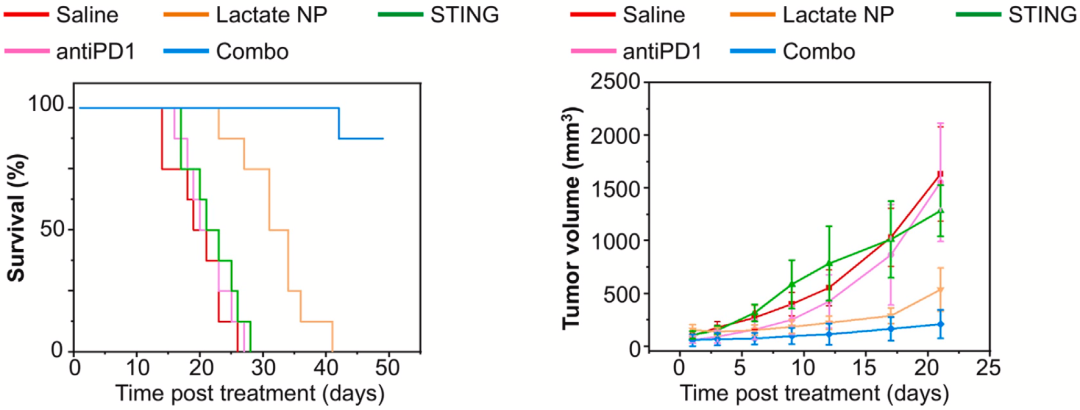
▲不同给药方式的SR-717治疗效果
从上述研究结果不难看出,吴小阳/Huang Jun团队开发的这个乳酸响应给药系统,利用肿瘤产生乳酸这一特征,大幅提升了药物对肿瘤的靶向性和治疗效果。
未来有必要基于这个给药系统开展更多的研究,让当下的抗癌药物能更好地作用于肿瘤。
参考文献:
[1].Bohn T, Rapp S, Luther N, et al. Tumor immunoevasion via acidosis-dependent induction of regulatory tumor-associated macrophages. Nat Immunol. 2018;19(12):1319-1329. doi:10.1038/s41590-018-0226-8
[2].Zhang D, Tang Z, Huang H, et al. Metabolic regulation of gene expression by histone lactylation. Nature. 2019;574(7779):575-580. doi:10.1038/s41586-019-1678-1
[3].Qian Y, Galan-Cobo A, Guijarro I, et al. MCT4-dependent lactate secretion suppresses antitumor immunity in LKB1-deficient lung adenocarcinoma. Cancer Cell. 2023;41(7):1363-1380.e7. doi:10.1016/j.ccell.2023.05.015
[4].Watson MJ, Vignali PDA, Mullett SJ, et al. Metabolic support of tumour-infiltrating regulatory T cells by lactic acid. Nature. 2021;591(7851):645-651. doi:10.1038/s41586-020-03045-2
[5].Kumagai S, Koyama S, Itahashi K, et al. Lactic acid promotes PD-1 expression in regulatory T cells in highly glycolytic tumor microenvironments. Cancer Cell. 2022;40(2):201-218.e9. doi:10.1016/j.ccell.2022.01.001
[6].Zong Z, Xie F, Wang S, et al. Alanyl-tRNA synthetase, AARS1, is a lactate sensor and lactyltransferase that lactylates p53 and contributes to tumorigenesis. Cell. 2024;187(10):2375-2392.e33. doi:10.1016/j.cell.2024.04.002
[7].Chen H, Li Y, Li H, et al. NBS1 lactylation is required for efficient DNA repair and chemotherapy resistance. Nature. 2024;631(8021):663-669. doi:10.1038/s41586-024-07620-9
[8].Zhang J, Pan T, Lee J, et al. Enabling tumor-specific drug delivery by targeting the Warburg effect of cancer. Cell Rep Med. Published online January 7, 2025. doi:10.1016/j.xcrm.2024.101920
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 总生存期(OS)提升5倍!实体瘤免疫治疗迎来重大突破 (2025-09-24)
- Nature:受蚯蚓启发,我国学者开发出新一代脑机接口功能电极——神经蠕虫 (2025-09-23)
- 不只是“脑子”的问题!Brain Behav Immun 新发现:乳酸代谢紊乱才是难治性精神分裂症的关键密码 (2025-09-23)
- 外卖盒/塑料杯产生的微塑料会进入大脑,或增加阿尔茨海默病风险 (2025-09-23)
- Int J Nanomedicine:预处理禽源间充质干细胞小囊泡,为卵巢早衰及激素下降提供新型纳米治疗方案 (2025-09-22)
- 东北农业大学最新研究登上Cell头条 (2025-09-22)
- Nature:细胞信号的“条形码”!科学家有望解锁癌症转移的秘密 (2025-09-22)
- 补充这种氨基酸,或能帮助减肥!《自然》研究发现身体产热新途径 (2025-09-22)
- Cell:细胞“返老还童”记—— LEC2如何“劫持”气孔发育通路以启动胚胎程序 (2025-09-22)
- Nature:蔡立慧团队揭示ABCA7变异驱动阿尔茨海默病风险的机制 (2025-09-21)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















