EBioMedicine:EZH2对FADS2的差异调控为卵巢癌治疗提供联合靶点,协同抑制显效 |
 |
来源:100医药网 2025-08-25 13:13
本研究发现EZH2差异调控FADS2转录变体,联合抑制EZH2和FADS2可诱导线粒体功能障碍和能量应激,对卵巢癌有更强抗肿瘤效果,为其提供潜在治疗策略。解析:标题包含杂志名称,点明研究核心机制(EZH2差异调控FADS2)、临床意义(提供联合靶点)及关键结果(协同抑制有效),与原文主题紧密关联,符合专业且具吸引力的要求。作为女性生殖系统中最具侵袭性和致命性的,其治疗一直是临床难题。多数患者确诊时已处于晚期,且对铂类化疗易产生耐药性,复发率高,预后极差。近年来,研究者们不断探索新的治疗靶点和策略,以期改善卵巢癌患者的生存状况。
近日,发表在EBioMedicine上的一项研究Differential regulation of FADS2 by EZH2 reveals a metabolic vulnerability in ovarian cancer treatment,揭示了EZH2与FADS2在卵巢癌中的调控关系及联合的潜力,为卵巢癌治疗带来了新的曙光。

该研究背景指出,卵巢癌具有异常脂质代谢的特征,而EZH2作为多梳抑制复合体2(PRC2)的催化亚基,通过经典的H3K27me3修饰及非经典机制发挥促肿瘤作用。尽管EZH2已被视为潜在的抗癌靶点,但其抑制剂在实体瘤中的治疗效果仍有限。
研究发现,EZH2对FADS2的转录变体具有差异化调控作用。EZH2敲除会使FADS2变体1(v1)在mRNA和蛋白水平均升高,而变体2/3(v2/3)则降低。ChIP-qPCR等实验表明,EZH2占据FADS2 v1和v2/3的启动子,但v2/3启动子处H3K27me3的富集显著低于v1启动子。此外,EZH2抑制剂会增加卵巢中全长FADS2 v1的表达和多不饱和脂肪酸(PUFA)的丰度。
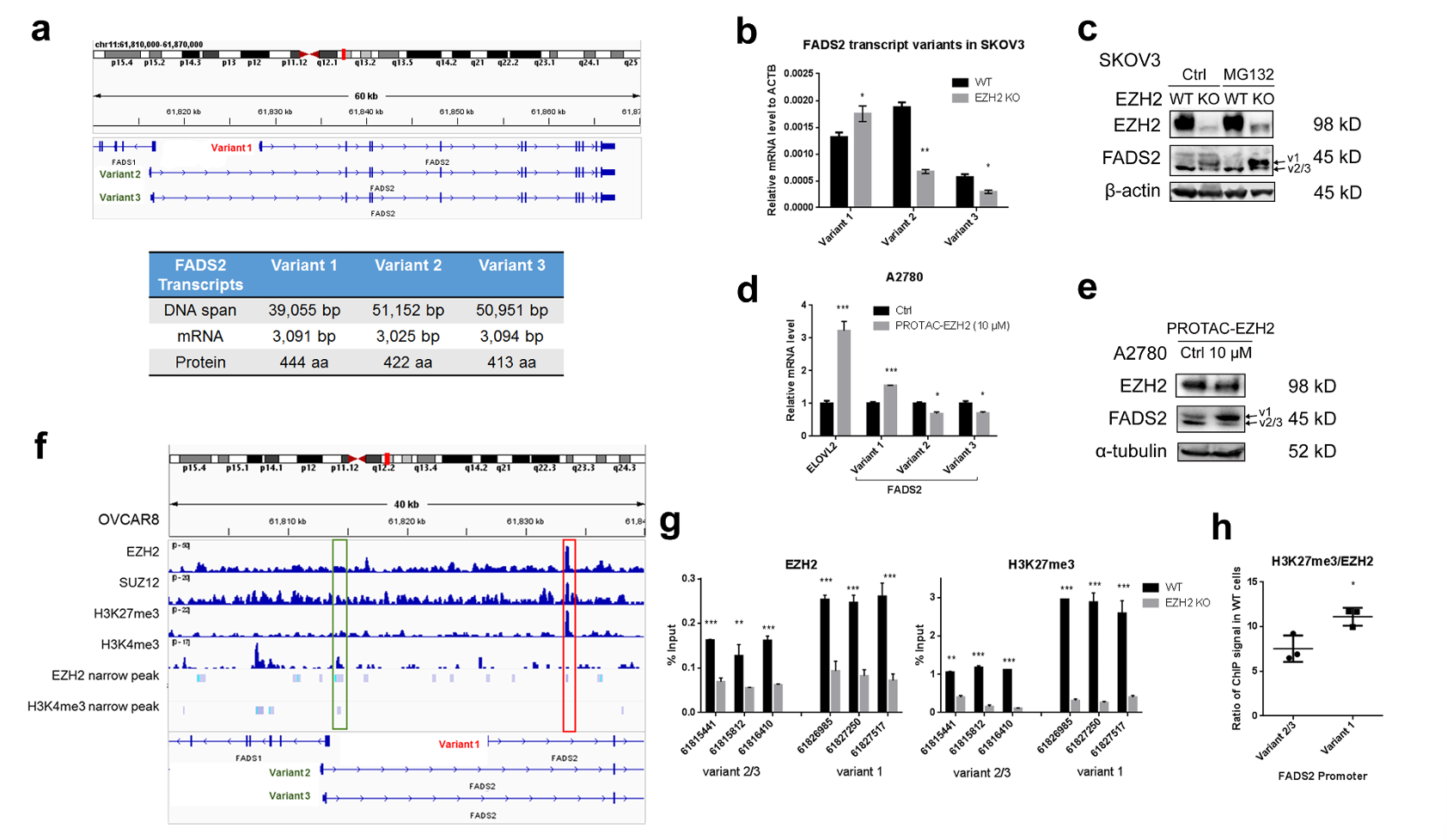
图1:EZH2对FADS2转录变体的差异化调控
临床数据显示,FADS2 v1/v2比值高与卵巢癌患者预后不良相关。通过shRNA或抑制剂靶向FADS2可降低EZH2水平,并使癌细胞对EZH2抑制剂敏感。体内外实验均证实,联合抑制EZH2和FADS2能诱导线粒体和能量应激,协同抑制肿瘤生长。
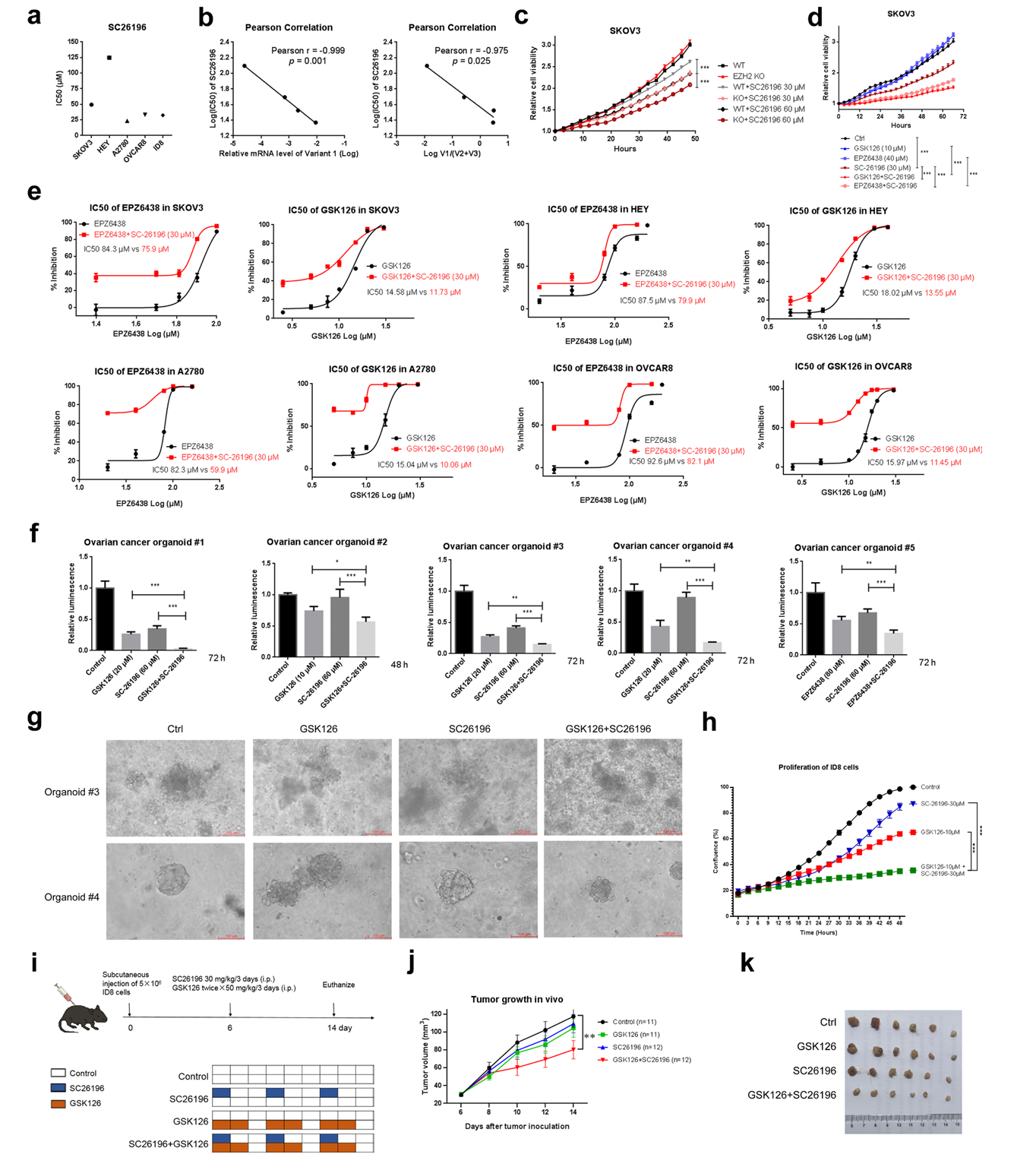
图2:联合靶向EZH2和FADS2增强对卵巢癌的抑制效果
机制研究方面,4D-DIA蛋白质组学、Seahorse实验等显示,联合治疗会抑制线粒体氧化磷酸化,减少ATP生成,激活AMPK信号通路,进而抑制mTOR介导的蛋白质合成,导致细胞周期停滞。同时,联合治疗还会下调Notch信号通路,协同抑制肿瘤进展。
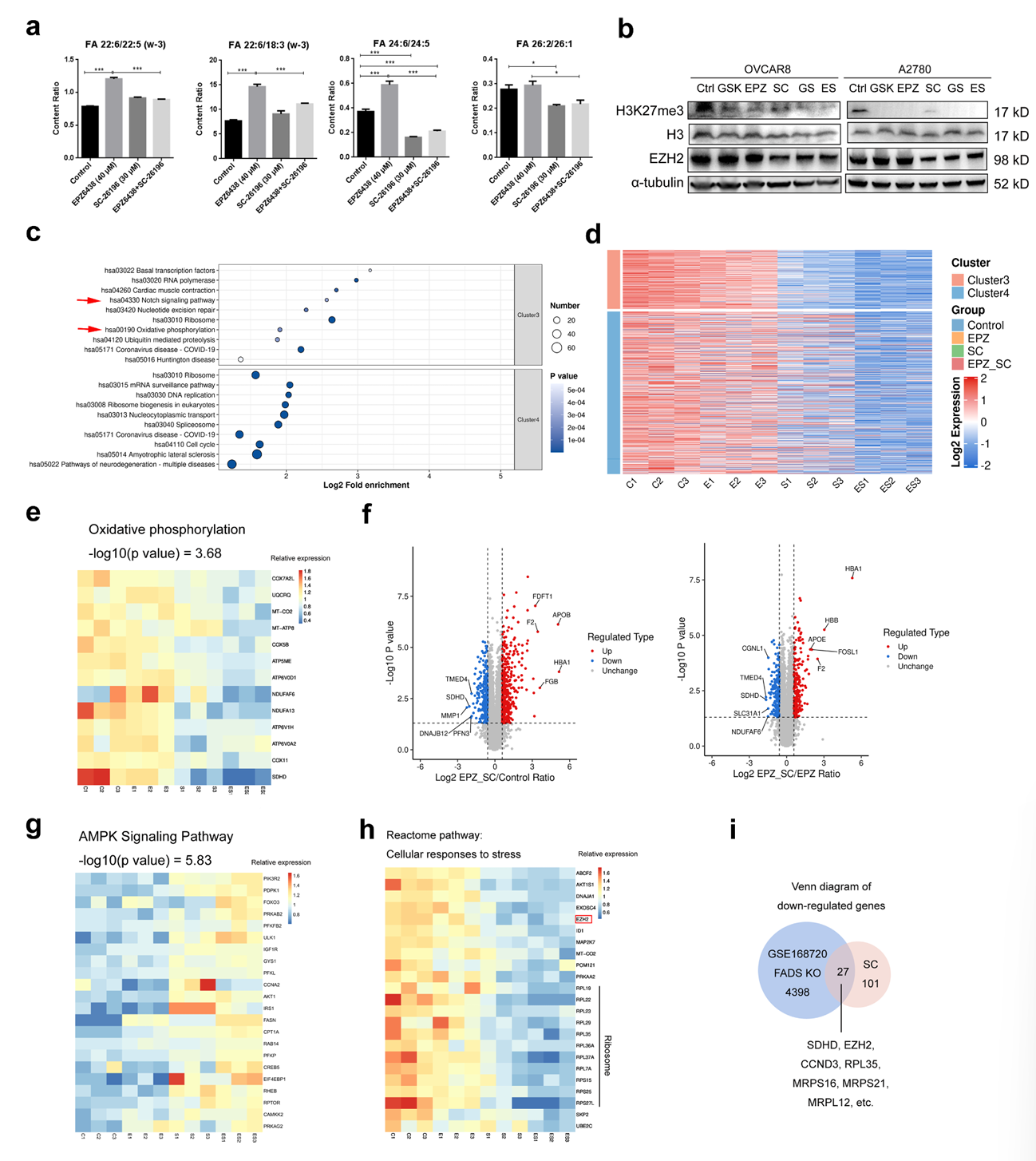
图3:EZH2和FADS2的双重抑制改变卵巢癌细胞的蛋白质组学特征
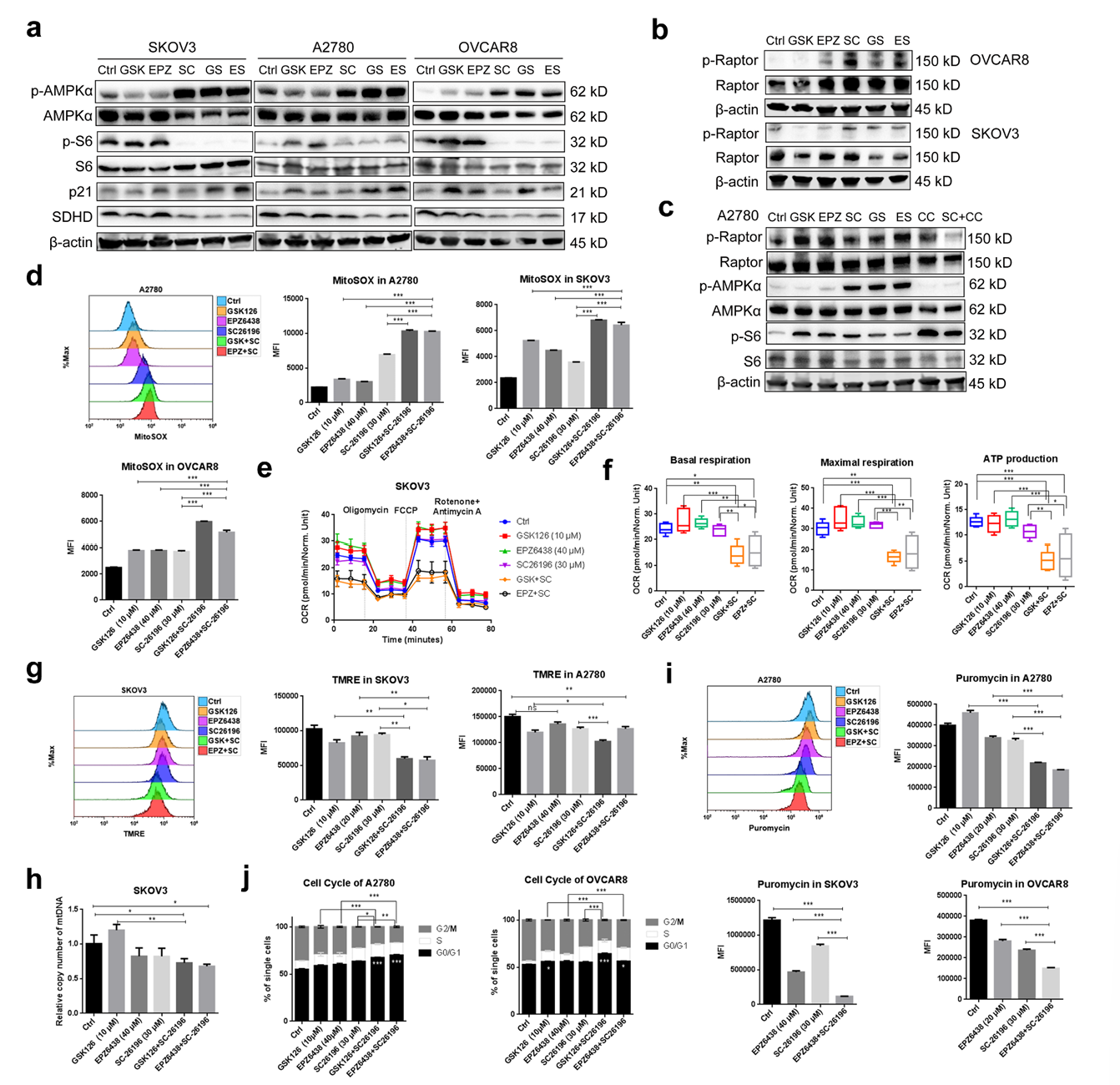
图4:联合靶向EZH2和FADS2损害卵巢癌细胞的线粒体功能
综上所述,这项研究揭示了EZH2通过差异化调控FADS2,在卵巢癌中形成代谢 vulnerability的机制。EZH2抑制会增加FADS2全长异构体的比例,而同时抑制EZH2和FADS2能通过诱导线粒体功能障碍和能量应激,产生更显著的抗肿瘤效果。这一发现不仅建立了表观遗传修饰与脂肪酸代谢之间的联系,更为卵巢癌提供了一种潜在的联合治疗策略,有望为临床治疗带来新的突破,让更多卵巢癌患者看到生存的希望。(100yiyao.com)
参考文献:
Guo Z, Wang Y, Song J, et al. Differential regulation of FADS2 by EZH2 reveals a metabolic vulnerability in ovarian cancer treatment.EBioMedicine. Published online August 15, 2025. doi:10.1016/j.ebiom.2025.105879
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature系列综述:西湖大学董晨院士系统总结CD8⁺T耗竭的调控因子 (2025-10-16)
- 由趋势观前沿:毕马威正式发布第三届生物科创领航50企业报告 (2025-10-15)
- 从“假基因”到“致病元凶”!Brain新研究:SSPOP基因复合杂合突变诱发儿童癫痫,多模型证实其功能与致病机制 (2025-10-15)
- Science:“吃不胖”的免疫学新解——T细胞胆固醇稳态是决定膳食脂肪吸收的关键 (2025-10-15)
- 迈威生物靶向 CDH17 ADC 创新药 7MW4911 临床试验申请获得 NMPA 批准 (2025-10-14)
- 西湖大学开发AI科学家,实现全自动科学发现,两周搞定人类科学家三年工作 (2025-10-14)
- Oncoscience:你的精子在“求救”?印度科学家发现,这些日常习惯正在偷走生育力! (2025-10-14)
- 腹痛便血反复?J Ethnopharmacol:“中医解法”被证实!芍药汤能精准激活肠干细胞,修复黏膜不反复 (2025-10-14)
- STTT:华西医院科学家发明可修复血脑屏障的纳米药物,可快速清除阿尔茨海默病毒蛋白、改善认知! (2025-10-14)
- Nature子刊:房颤竟是一种自身免疫疾病? (2025-10-14)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















