8月Nature杂志重磅级亮点研究成果解读! |
 |
时光总是在不经意间匆匆流过,转眼间8月份即将结束,在即将过去的8月里,Nature杂志又有哪些亮点研究值得一读呢?小编对相关亮点文章进行了筛选整理,分享给大家!
【1】
doi:10.1038/s41586-025-09335-x
阿尔兹海默病(AD,Alzheimer s Disease)是全球最常见的神经退行性疾病之一,其发病率随着人口老龄化而不断增加。据WHO数据显示,全球约有5000万阿尔兹海默病患者,预计到2050年这一数字将会翻倍。阿尔兹海默病的特征性病理变化包括脑内淀粉样斑块(A )的沉积和神经原纤维缠结(tau蛋白过度磷酸化)。尽管科学家们对AD的发病机制进行了大量研究,但目前仍缺乏有效的治疗方法。
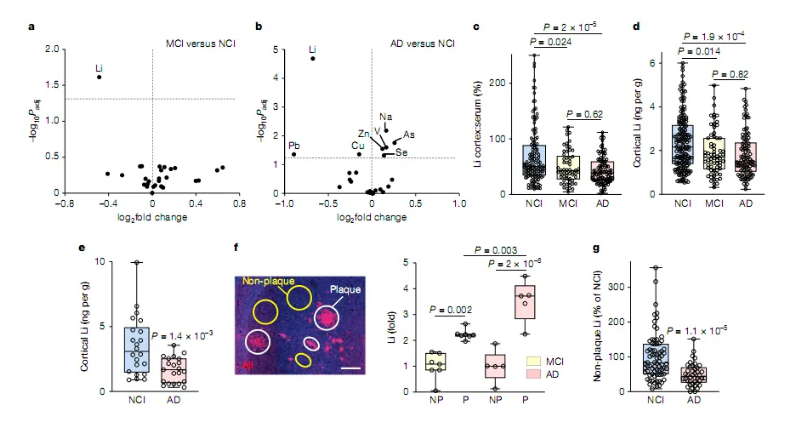
锂缺乏和阿尔兹海默病发生的开始
近年来,锂作为一种潜在的治疗手段引起了研究者的关注,锂在临床上主要用于治疗双相情感障碍,但其在神经保护和认知功能维持方面的作用也逐渐被发现。日前,一篇发表在国际杂志Nature上题为 Lithium deficiency and the onset of Alzheimer s disease 的研究报告中,来自哈佛医学院等机构的科学家们揭示了锂在大脑中的生理作用,阐释了锂缺乏与阿尔兹海默病发病机制之间的潜在联系。
文章中,研究者首先分析了健康老年人和轻度认知障碍(MCI,Mild Cognitive Impairment)及阿尔兹海默病患者的脑组织样本,结果发现,与健康对照组相比,MCI和AD患者的前额叶皮层中锂的水平会显著降低;这种锂缺乏与A 沉积和tau蛋白过度磷酸化密切相关,而且锂缺乏会激活GSK3 激酶,GSK3 酶在A 和tau病理中均发挥着重要作用。
【2】
doi:10.1038/s41586-025-09310-6
在当今全球健康领域,自身免疫性疾病和慢性炎症性疾病正逐渐成为影响人类健康的重大挑战,系统性红斑(SLE,systemic lupus erythematosus)等自身免疫性疾病的发病机制与体内免疫系统对自身核酸的异常识别密切相关。如今,越来越多的证据表明,RNA的异常修饰可能会触发免疫系统的过度激活从而引发炎症反应,近年来,RNA糖基化作为一种新兴的RNA修饰方式,引起了科学家们的广泛关注,这种修饰涉及在RNA分子上添加N-糖链,尤其是在3-(3-氨基-3-羧丙基)尿嘧啶(acp3U)这一特殊位点上;然而,RNA糖基化修饰的具体功能及其在免疫反应中的作用尚不清楚。
近日,一篇发表在国际杂志Nature上题为 RNA N-glycosylation enables immune evasion and homeostatic efferocytosis 的研究报告中,来自康涅狄格大学健康医学院等机构的科学家们通过研究揭示了RNA糖基化如何通过调节免疫系统来影响细胞凋亡后的清除过程及自身免疫性疾病的发病机制。
文章中,研究人员通过一系列实验揭示了RNA糖基化在免疫逃逸和细胞凋亡后清除过程中的重要作用;首先他们从HeLa细胞中分离出小RNA,并使用PNGase F酶去除RNA上的N-糖链,结果显示,去糖基化的小RNA能强烈激活RAW巨噬细胞并诱导I型干扰素(IFN )产生,而未经处理的小RNA则无此效果。进一步的实验表明,这种免疫激活作用依赖于Toll样受体3(TLR3)和Toll样受体7(TLR7),这两种受体能分别识别双链RNA和单链RNA。研究人员还发现,细胞表面的糖基化RNA在细胞凋亡后被巨噬细胞吞噬时能阻止内质网RNA传感器的激活从而促进细胞凋亡后的非炎症性清除,这一过程对于维持组织稳态至关重要。
【3】
doi:10.1038/s41586-025-09299-y
据世界卫生组织,每年全球新增癌症病例约1800万,其中肺癌和胰腺癌更是以其高发病率和高死亡率成为人类健康的重大威胁。肺癌是全球癌症相关死亡的首要原因,每年约有200万人死于肺癌,而胰腺癌则因其早期症状不明显、进展迅速,5年生存率不足10%;基于这一背景,寻找新型有效的治疗策略就显得尤为迫切。
近日,一篇发表在国际杂志Nature上题为 NSD2 inhibitors rewire chromatin to treat lung and pancreatic cancers 的研究报告中,来自斯坦福大学等机构的科学家们通过研究揭示了一种针对NSD2的抑制剂,有望为肺癌和胰腺癌的治疗带来新的希望。
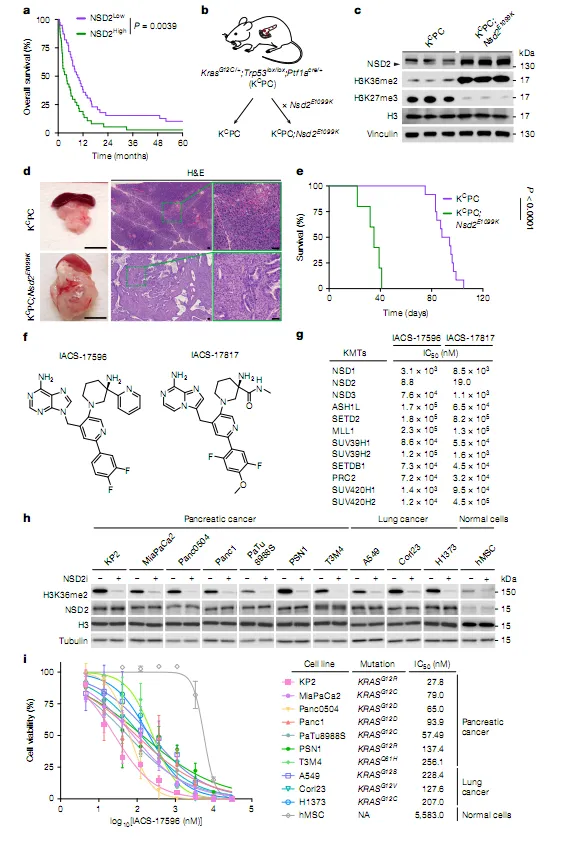
NSD2能加速恶性PDAC和NSD2i的功能性表征
NSD2是一种关键的表观遗传修饰酶,其能通过催化H3K36me2修饰来调控基因表达和染色质状态。在多种癌症中,NSD2的异常激活与肿瘤的发生和发展密切相关,然而此前针对NSD2的药物开发一直面临挑战,缺乏有效的临床级小分子抑制剂。这项研究中,研究人员成功开发了一系列高选择性、高活性的NSD2催化抑制剂(NSD2i),并系统评估了其在KRAS驱动的肺癌和胰腺癌模型中的治疗效果。
【4】
doi:10.1038/s41586-025-09272-9
爸妈给的基因,到底管多少事? 体检报告上那一串箭头和红字总让人忍不住嘀咕。全球慢性病地图冷冰冰地提醒我们,每10秒就有人被心疾病带走,每30秒就新增一位癌症患者;在英国,三分之二的成年人长期与至少一种慢病共舞,基因、环境与运气,到底谁在发牌?近日,一篇发表在国际杂志Nature上题为 Whole-genome sequencing of 490,640 UK Biobank participants 的重磅研究就把490,640名英国人的基因组一次性摊在桌面 高清无码,答案终于来了。
故事的主角是UK Biobank,一个把 深度八卦 做到极致的公共队列,其联合阿斯利康、安进、葛兰素史克、强生、Illumina、Sanger研究所等,把近50万名志愿者的30亿个DNA字母用NovaSeq 6000读了32.5遍,确保一个错别字都不放过。结果科学家挖出了15亿个变异,比上一代芯片技术暴涨18.8倍,比传统只测外显子的 外显子组 更是飙升40倍 如果过去的基因组地图是一张模糊的JPEG,现在直接升级成4K蓝光原盘。
别以为这只是量变,过去我们盯着外显子,就像只翻菜单不看后厨,这次把厨房也翻了个底朝天;原来,13.7%的蛋白编码区突变在外显子组里根本找不到,90%的非编码 暗物质 第一次被拉到聚光灯下。研究人员发现,这些隐形段落里藏着甲状腺功能减退、等常见病的开关,而50多万个结构变异(50个字母以上的大片段插入、缺失、重复)虽然70%都极其罕见,却平均能影响每人3.6兆的DNA长度,威力堪比一整部《权游》全集。
更有趣的是,同样的突变,放到不同祖先背景里,结局可以天差地别,研究人员把人群分成非洲、东亚、南亚、非芬兰欧洲、阿什肯纳兹犹太五大 血统战队 。在非洲血统里,镰刀型突变rs334的频率高达6.26%,是欧洲的1500倍,因为其能预防疟疾;南亚人携带 -地中海贫血突变的比例又是欧洲的5000倍,而欧洲常见的HBB无义突变,到了南亚和非洲几乎绝迹,一句话,你的祖先当年在哪片大陆打怪升级,决定了你今天血条的长短。
【5】
doi:10.1038/s41586-025-09461-6
诸如泰-萨克斯病(Tay-Sachs)和桑霍夫病(Sandhoff)等遗传性脑病是一类罕见但极其严重的神经退行性疾病,通常在患者生命的头几年内导致死亡,这些疾病属于溶酶体贮积症,是由于溶酶体酶缺陷导致细胞内废物积累而引发的,尽管这些疾病发病率较低,但对患者及其家庭的影响却是毁灭性的。有数据显示,泰-萨克斯病在阿什肯纳兹犹太人新生儿中的发病率约为1/3700,而桑霍夫病则更为罕见,这些疾病目前尚无有效治疗方法,患者通常在症状出现后迅速恶化,最终因神经退化而死亡。
近年来,细胞替代疗法作为一种潜在的治疗策略被提出,即通过移植健康的细胞来替换受损的脑细胞来减缓或阻止神经退化;然而,这种方法面临着诸多挑战,包括脑部移植细胞的低嵌合率以及移植细胞攻击健康组织的移植物抗宿主病(GVHD)。
近日,一篇发表在国际杂志Nature上题为 Therapeutic genetic restoration through allogeneic brain microglia replacement 的研究报告中,来自斯坦福大学医学院等机构的科学家们开发了一种新方法,其能在不进行全身性毒性预处理的情况下,将超过一半的受损小胶质细胞替换为非基因匹配的前体细胞,这一突破性进展为治疗这些罕见疾病带来了新的希望。
这项研究的核心是开发一种脑部限制性的高效率小胶质细胞替代方法,研究人员发现,与之前假设不同,造血并非是重新填充脑环境髓样细胞所必需的;相反,Sca1定向前体细胞(Sca1-commited progenitor cells)在脑内注射后能够高效地替代小胶质细胞,这一发现就能促使研究人员开发出一种脑部限制性的预处理方法,避免了长期的外周嵌合,从而消除了移植物抗宿主病等并发症。
【6】
doi:10.1038/s41586-025-09421-0
你是否曾经疑惑,为什么有些人似乎天生就不容易感染某些细菌?或者为什么有些人即使接触了病毒也能迅速恢复?这背后可能与我们体内一群 神秘 的免疫细胞 B-1a细胞有关。长久以来,科学家们甚至对 人类是否真的拥有这类细胞 争论不休。如今,一篇发表在国际杂志Nature上题为 TCF1 and LEF1 promote B-1a cell homeostasis and regulatory function 的研究报告中,来自澳大利亚国立大学等机构的科学家们通过研究不仅确认了人类B-1a细胞的存在,还揭示了两个关键转录因子 TCF1和LEF1 如何像 指挥官 一样调控这群细胞的生存与功能,相关研究不仅解开了免疫学中的一个谜团,更为未来治疗自身免疫疾病、慢性感染甚至癌症提供了新思路。
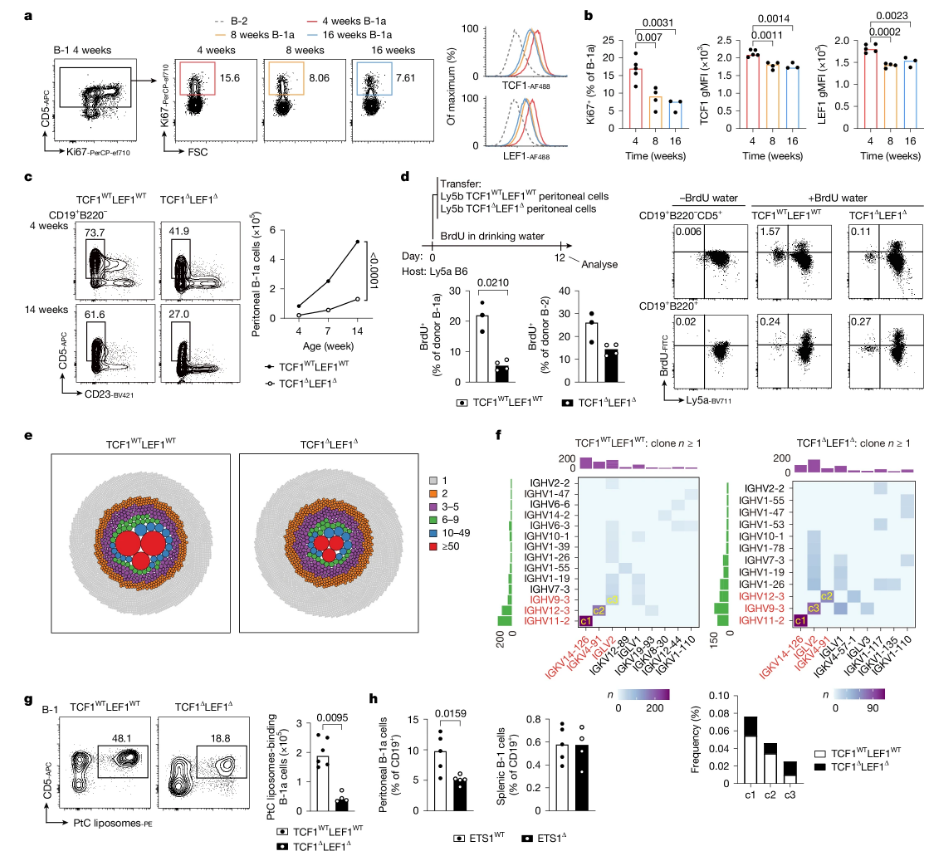
TCF1和LEF1是B-1a细胞自我更新所需要的
B-1a细胞是一类先天免疫样B细胞,其主要分布在胸腔、腹腔等浆膜腔中,能快速产生天然抗体来识别细菌、病毒等病原体;同时其还能分泌诸如IL-10等抗炎因子并表现出 免疫调节 功能,且有助于防止过度炎症反应和自身免疫疾病。然而,这类细胞在人体中是否真实存在、如何维持、功能如何调控,一直是免疫学领域的争议焦点。
这项研究中,研究人员旨在揭示B-1a细胞背后的 指挥系统 ,他们重点聚焦于两个转录因子TCF1和LEF1,这两个因子在T细胞和干细胞中已知能调控 干细胞特性 ,但在B细胞中的作用尚不明确,因此研究人员就想知道TCF1和LEF1是否也在B-1a细胞中表达?其是否影响B-1a的发育、维持与功能?
【7】
doi:10.1038/s41586-025-09326-y
在当今快节奏的生活中,慢性疼痛似乎已经成了许多人难以摆脱的 影子 ,无论是长时间伏案工作后的腰酸背痛,还是因疾病引发的持续性不适,慢性疼痛不仅影响着我们的,还给社会带来了沉重的经济负担。有数据显示,全球约有五分之一的成年人受到慢性疼痛的困扰,而慢性疼痛更是全球致残的首要原因。现有的治疗手段往往因疗效有限、耐受性差等问题难以满足需求。那么,有没有一种更有效、更安全的治疗方法呢?
近日,一篇发表在国际杂志Nature上题为 SLC45A4 is a pain gene encoding a neuronal polyamine transporter 的研究报告中,来自牛津大学等机构的科学家们通过研究发现了一种名为SLC45A4的基因,其能编码一种神经元多胺转运蛋白且与慢性疼痛密切相关。这一发现不仅为理解疼痛的分子机制提供了新的视角,还可能为开发新型镇痛药物开辟道路。
慢性疼痛的成因复杂,其中一个重要因素是伤害性感受器(即能感知伤害性刺激的感觉神经元)及其投射的中枢伤害性回路兴奋性增强,这种过度活跃会导致疼痛信号持续传递至大脑,进而引发慢性疼痛。然而,目前对于调节这些神经元兴奋性的分子机制仍不完全清楚。这项研究中,研究人员就旨在探索SLC45A4基因在疼痛感知中的作用,并揭示其编码的多胺转运蛋白如何影响神经元的兴奋性,为开发新的镇痛策略提供理论依据。
研究人员首先通过全基因组关联研究()分析了来自英国生物银行(UKB)中 132,552 名欧洲血统参与者的慢性疼痛数据,发现SLC45A4基因中的某些单核苷酸变异(SNVs)与疼痛强度显著相关,其中位于该基因内含子的 rs10625280 和错义变异 rs3739238(p.Asn718Asp)关联性尤为显著。随后,这些变异在百万退伍军人计划(MVP)的欧洲血统人群(约 60 万参与者)和芬兰基因组计划(FinnGen)中均得到验证,且效应方向一致,证实了SLC45A4与疼痛感知的遗传关联。
【8】
doi:10.1038/s41586-025-09433-w
如今,癌症依然是人类健康的重大威胁之一,尽管医学技术不断进步,但癌症的复杂性和多样性使得治疗面临重重挑战。近年来,随着对癌症生物学机制的深入研究,科学家们逐渐发现,细胞周期的异常调控是癌症发生和发展的重要因素之一。细胞周期是指细胞从一次分裂结束到下一次分裂结束所经历的全过程,其受到多种蛋白质的精细调控;其中,细胞周期蛋白(Cyclin)和细胞周期蛋白依赖性激酶(CDK)的异常激活常常会导致细胞过度增殖进而引发癌症。因此,开发针对细胞周期调控的新型药物成为了癌症治疗领域的前沿热点。
近日,一篇发表在国际杂志Nature上题为 Targeting G1 S-checkpoint-compromised cancers with cyclin A/B RxL inhibitors 的研究报告中,来自哈佛医学院等机构的科学家们通过研究开发了一种治疗小细胞肺癌的新型策略,有望进一步推动临床试验的开展。文章中,研究者开发了一种新型的细胞周期抑制剂,尤其是针对细胞周期蛋白A和B的RxL基序抑制剂。
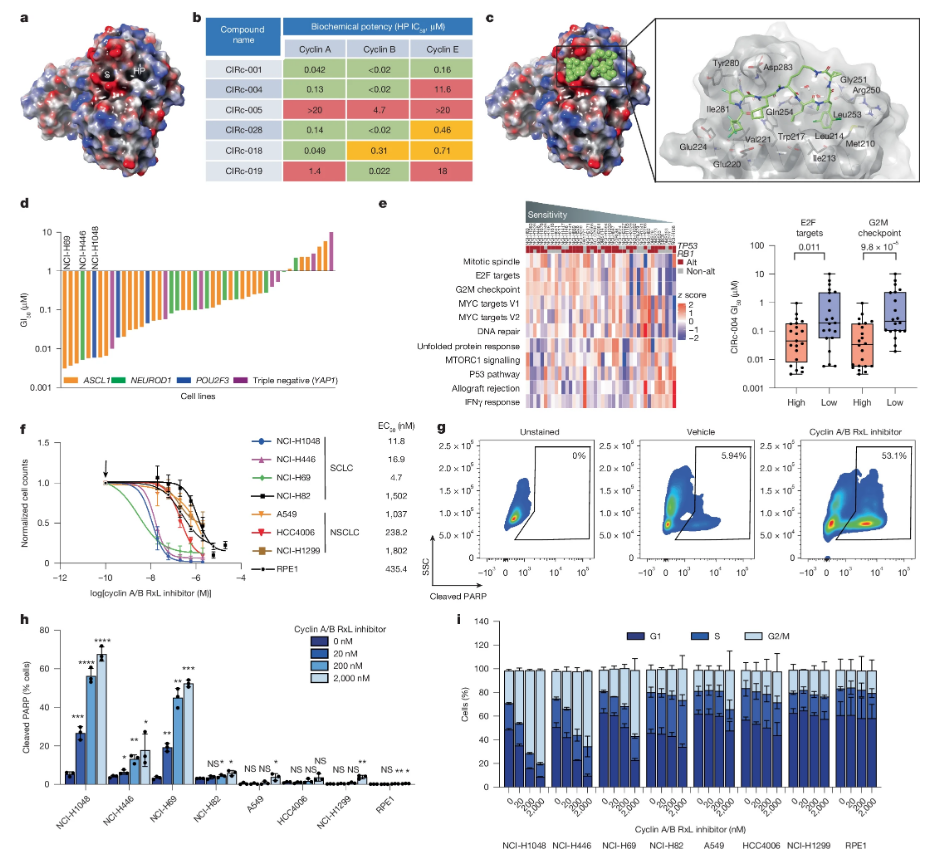
细胞周期蛋白A/B RxL抑制剂或能诱导具有高E2F活性的凋亡
细胞周期蛋白A和B在细胞周期的调控中起着关键作用,其能通过与特定的底物蛋白相互作用来调节细胞的增殖和分裂。在诸如小细胞肺癌(SCLC)等某些癌症类型中,细胞周期蛋白A和B的活性异常升高从而就会导致细胞过度增殖和肿瘤的形成。因此,抑制细胞周期蛋白A和B的活性有望成为一种有效的癌症治疗策略。
【9】
doi:10.1038/s41586-025-09370-8
你是否能想象,癌症这一无情的病魔,不仅无情地侵蚀人体器官,还能狡黠地 操控 神经系统,进而使免疫治疗这一抗癌利器失去效力?这并非科幻小说中的情节,而是一项前沿科学研究揭示的惊人事实。近日,发表于国际顶尖杂志Nature上题为 Cancer-induced nerve injury promotes resistance to anti-PD-1 therapy 的研究报告,由德克萨斯大学 MD 安德森癌症研究中心等全球 30 多家顶尖机构携手合作完成,为我们揭开了全新的抗癌耐药机制 癌细胞能够主动损害机体周围神经,引发慢性炎症,进而诱导免疫系统 叛变 ,最终致使免疫治疗宣告失败。这项意义非凡的研究,不但阐释了部分患者对 PD-1 抑制剂治疗无反应的深层原因,更为逆转耐药提供了一系列创新策略。
研究人员最初将目光聚焦于 神经周围侵犯 (PNI,Perineural Invasion)这一现象。早在多年前,临床医生便已察觉,当癌细胞包绕或侵入神经时,患者的预后往往不容乐观,尤其是在皮肤鳞癌、瘤、等多种癌症类型中,PNI 更是作为显著的 不良预后指标 频繁出现。然而,长久以来,神经遭受癌细胞侵犯后究竟发生了何种变化,始终是未解之谜。
通过对 56 名接受 PD-1 抑制剂治疗的皮肤癌患者展开深入分析,研究人员惊异地发现,在治疗无响应的患者群体中,高达 50% 存在 PNI 现象;而在治疗有响应的患者里,这一比例仅为 15%。这一数据清晰表明,神经被侵犯的患者,对免疫治疗产生耐药性的可能性显著增加。进一步深入探究后,研究者们发现,这些受侵犯的神经呈现出 受伤状态 ,它们会大量高表达 ATF3 等损伤标志物,仿佛在绝望地发出 SOS 求救信号。由此可见,神经损伤与机体对抗 PD-1 疗法的耐受性之间,存在着直接且紧密的关联。
【10】
doi:10.1038/s41586-025-09411-2
在当今社会,癌症依然是人类健康的重大威胁之一,其中胶质母细胞瘤(GBM,Glioblastoma)因其高度侵袭性和治疗抵抗性,成为了神经科学领域中最棘手的难题之一。尽管医学技术不断进步,但胶质母细胞瘤患者的中位生存期仍仅为12至18个月,且常伴有严重的身体和认知,这一残酷的现实促使科学家们不断探索新的治疗方法和研究方向。
近日,一篇发表在国际杂志Nature上题为 Axonal injury is a targetable driver of glioblastoma progression 的研究报告中,来自伦敦大学学院癌症研究所等机构的科学家们通过研究发现,轴突损伤可能是胶质母细胞瘤进展的关键驱动因素,而抑制这一过程或许能成为治疗胶质母细胞瘤的新策略。
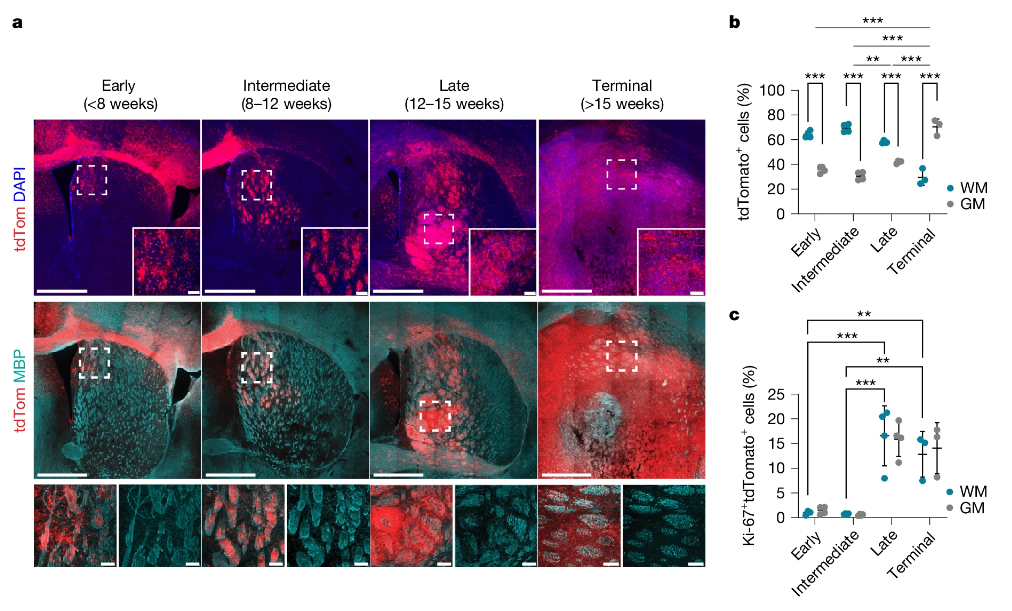
肿瘤的发展会优先出现在大脑白质中
胶质母细胞瘤的早期阶段研究相对较少,因为晚期肿瘤的复杂性掩盖了早期阶段的潜在治疗靶点,早期如何在大脑中扩散及其如何引发肿瘤进展一直是科学家们关注的焦点。这项研究中,研究人员旨在探索轴突损伤在胶质母细胞瘤早期发展中的作用并验证抑制轴突损伤是否能减缓肿瘤进展,这一发现不仅有助于我们更好地理解胶质母细胞瘤的发病机制,还可能为开发新的治疗方法提供理论基础。文章中,研究人员使用了包括小鼠模型和患者来源的异种移植(PDX)模型等多种实验模型进行研究;在小鼠模型中,他们通过基因编辑技术诱导胶质母细胞瘤的发生并观察肿瘤细胞在大脑中的分布和进展;同时利用空间转录组学技术分析肿瘤微环境中的基因表达变化;还通过手术损伤小鼠的脑组织来模拟轴突损伤,并观察这种损伤对肿瘤进展的影响。(100yiyao.com)
更多精彩盘点:
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- PNAS:精子也“飙车”?科学家发现能量开关,有望颠覆不孕与避孕未来 (2025-10-16)
- Cell:小胶质细胞-星形胶质细胞交谈调节突触重塑 (2025-10-16)
- 香港西医病院开院首年将提供门诊及日间住院等服务 (2025-10-16)
- 国度药监局对于刊出氯雷他定片等80个药品注册证书的布告 (2025-10-16)
- 《自然·神经科学》:从身到心,一次改善!单剂量裸盖菇素可快速且持续地缓解慢性疼痛小鼠痛觉异常和情绪障碍 (2025-10-16)
- 山东优化养老服务网络 变“养老”为“享老” (2025-10-16)
- Nature Medicine:当新生儿筛查遇上基因组测序,我们准备好了吗? (2025-10-16)
- 颜宁团队连发两篇论文:解析“酷寻”策略发现的全新糖纤维结构,并开发绝对手性判定新算法 (2025-10-16)
- Cell:里程碑式突破!I/IIa期临床试验证实hESC衍生细胞移植可安全并有效地重建帕金森病患者的多巴胺能系统 (2025-10-16)
- 抑郁不只是“情绪感冒”!Science 子刊揭密:大脑糖链“脱落”才是关键,靶向修复或破治疗困局 (2025-10-15)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















