Nature:新研究揭示了睡眠期间大脑两个半球之间的竞争 |
 |
来源:100医药网原创 2023-03-28 10:03
在一项新的研究中,研究人员通过研究澳洲鬃狮蜥的睡眠,发现在睡眠的一个阶段,澳洲鬃狮蜥大脑的两个半球互相竞争,一方将其活动强加于另一方,直到占主导地位的半球切换到另一方,整个晚上交替进行。人类是左右对称的。因此,我们的大脑由两个半球组成,这两个半球通过穿过中线的特殊纤维束相互交流。虽然每个半球都倾向于处理身体另一侧的感官(视觉、听觉、触觉)和运动控制,但由于这两个半球之间的不断交流,我们一般不会意识到这种功能的划分。在人类中,这两个大脑半球也专门负责某些功能,比如语言区通常位于大脑左半球。
大多数动物(鸟类、爬行动物、两栖动物、鱼类、昆虫、软体动物等)和人类一样,都是左右对称的,并拥有左右对称的大脑。在一项新的研究中,德国福马克斯-普朗克脑科研究所的Lorenz Fenk、Luis Riquelme和Gilles Laurent研究了一种爬行动物---澳洲鬃狮蜥(Pogona vitticeps)---的睡眠,发现在睡眠的一个阶段,澳洲鬃狮蜥大脑的两个半球互相竞争,一方将其活动强加于另一方,直到占主导地位的半球切换到另一方,整个晚上交替进行。相关研究结果于2023年3月22日在线发表在Nature期刊上,论文标题为 Interhemispheric competition during sleep 。

Fenk解释说, 澳洲鬃狮蜥的睡眠分为两种状态,与包括人类在内的哺乳动物所描述的状态相似:一个阶段是所谓的慢波睡眠,其得名因为脑电图显示低频波;第二个阶段快速眼动(Rapid Eye Movement,REM)睡眠,在此阶段,脑电图与清醒状态时的记录相似,眼睛往往在眼睑下做抽搐运动,而身体则处于麻痹状态。
在人类中,睡眠开始于一个较长的慢波阶段(约60分钟),然后是5~10分钟的REM睡眠,这种交替的循环再次开始,每晚5~7次。随着夜晚的进行,每个睡眠周期中的REM睡眠部分会增加。在澳洲鬃狮蜥中,睡眠周期要短得多(不到2分钟),这两种睡眠状态的持续时间相等(每种状态45~60秒),贯穿整个晚上。澳洲鬃狮蜥每晚要经历250~350个这样的睡眠周期,在它的慢波睡眠和REM睡眠之间有规律地交替进行。
通过同时记录澳洲鬃狮蜥大脑两侧的同一区域(称为屏状核)的神经元活动,这些作者发现在睡眠的慢波阶段,每一半球都独立于另一个半球运作。然而,令他们惊讶的是,在REM睡眠阶段,这两个半球变得精确同步,但这两个半球之间有20毫秒的极短延迟。更令人惊讶的是,他们发现领先另一个半球20毫秒的半球在每个睡眠周期中平均在左半球和右半球之间切换一次。
通过比较REM睡眠期间在左、右屏状核(claustrum)上记录的信号强度,他们还观察到,活动较强的半球通常是领先的半球。这一点---连同他们论文中提出的其他证据--表明大脑的两个半球在REM睡眠期间相互竞争,但在慢波睡眠期间不竞争,而且在竞争时,较强的半球将它的活动强加于另一个半球。这种形式的竞争被称为 赢家通吃 。
有趣的是,尽管左、右半球在整个晚上起主导作用的时间大致相等(大约各占睡眠周期的一半),但这两个半球之间的切换并不完全随着每个睡眠周期而发生。此外,在晚上的最后几个小时,这两个半球之间的切换变得不那么频繁,在许多睡眠周期中,一个半球主导另一个半球,然后将主导地位让给另一个半球,同样是在许多连续的睡眠周期中。
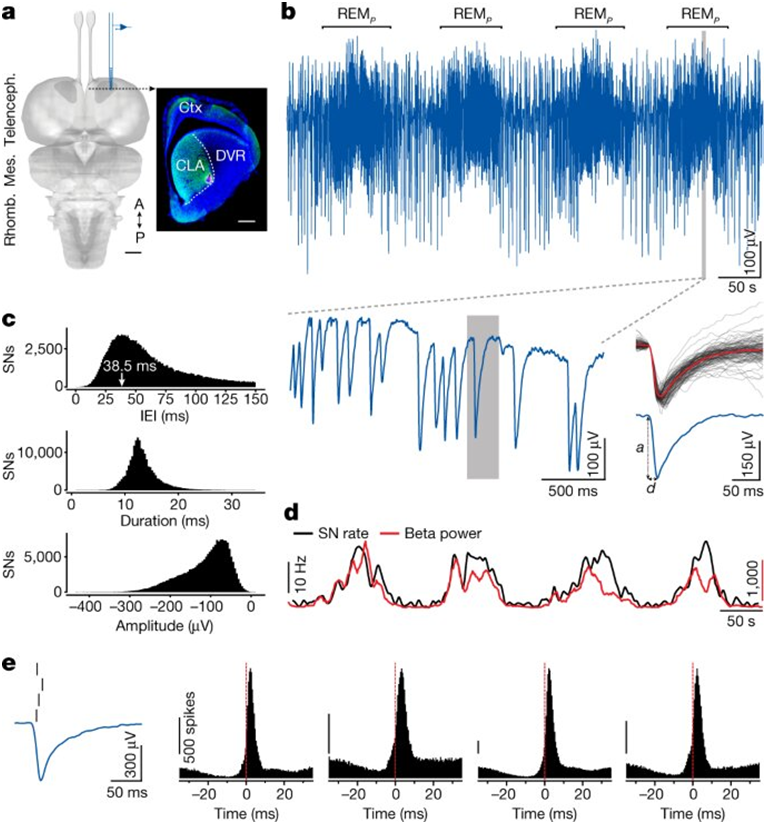
图片来自Nature, 2023, doi:10.1038/s41586-023-05827-w。
Laurent说, 这表明存在几个睡眠控制回路并相互作用,每个回路都有不同的时间尺度,其中一些时间尺度在整个晚上发生系统性演变;这表明无论睡眠在这些动物中发挥什么功能,不同的机制可能在晚上的早期和晚期发挥作用,产生不同的后果。
在努力了解大脑两个半球在REM睡眠期间是如何相互作用和竞争的过程中,这些作者发现这种竞争并不是由于左、右屏状核之间的直接相互作用,而是由于在大脑更深处的中脑和后脑交界处发现的回路。这些所谓的峡部回路(isthmic circuit)在所有脊椎动物中都有,包括哺乳动物和人类,并且在鸟类中得到了特别好的研究。在鸟类中,它们已被证明对清醒的鸟类(猫头鹰和鸽子)的某些形式的视觉注意很重要。通过仅破坏澳洲鬃狮蜥大脑的一个半球中这些峡部回路的一个组成部分进,Fenk及其同事们能够取消半球主导地位的定期切换,使完整的一个半球在整个晚上(连续多个晚上)支配另一个半球。
虽然这项新研究中涉及的回路组成部分(屏状核、中脑和峡部)存在于包括人类在内的哺乳动物中,但目前还不知道在人类的REM睡眠期间是否也会发生类似的竞争性相互作用。睡眠的机制和功能是复杂的,在任何动物中仍然知之甚少。在爬行动物中的这些新结果为睡眠动力学和功能的重要问题增加了新的复杂性。( 100yiyao.com)
参考资料:
Lorenz A. Fenk et al. . Nature, 2023, doi:10.1038/s41586-023-05827-w.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 终结持续25年的争论!娄智勇/饶子和等团队合作最新Cell (2025-10-26)
- 上海药物所×临港实验室合作发表Cell论文:基于结构发现新型抗抑郁小分子 (2025-10-26)
- Mol Cancer:阻断甲状腺激素受体为前列腺癌治疗提供了新的途径 (2025-10-26)
- Science子刊:卞修武团队发现增强CAR-T细胞抗肿瘤效果的基因修饰策略 (2025-10-26)
- Nature Biotechnology:直击囊胚“混沌期”——长时程活体成像首次捕捉人类囊胚的染色体分离灾难 (2025-10-26)
- JNCCN:戒烟也应当是癌症治疗的一环!13万名癌症患者数据分析结果显示,癌症确诊后及时戒烟可大幅降低死亡风险,改善手术预后 (2025-10-26)
- NEJM:人工视网膜,帮助老年性黄斑变性患者恢复视力 (2025-10-25)
- 华中师范大学最新Cell子刊论文:开发治疗白血病的多肽类药物 (2025-10-25)
- 《科学》:膳食脂肪重塑昼夜节律!加州大学科学家发现,饮食中不饱和脂肪酸比例会影响昼夜节律,是人体生物钟与季节匹配与否的关键 (2025-10-25)
- 河南中州实验室发表Nature Metabolism论文:揭开大脑髓鞘再生修复的关键 (2025-10-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















