石药:40款1类新药亮眼,11个种类抢首仿 |
 |
医药网7月14日讯 近日,石药集团动静频发:枸橼酸托法替布片获批临盆并视同过评、1类新药SYSA1801初次获批临床......近年来,公司不时加年夜研发投入,今朝有40款1类新药处于获批临床及以上阶段,2款立异药上市期近,DPP-4克制剂、FLT3克制剂等将陆续报产;在审的新分类报产仿造药中,11个种类冲刺首仿,此中5个为独家报告;一致性评估方面,今朝公司有56个种类过评(19个首家),3个种类中选第五批集采。
40款1类新药亮眼,“固守”高端制剂
近日,石药集团新药研发有新停顿:1类新药SYSA1801、高端制剂打针用西罗莫司(白卵白联合型)初次获批临床、生物相似药帕妥珠单抗打针液报告临床......米内网数据显示,今朝石药集团处于获批临床及以上阶段的1类新药有40个(报告新顺应症不计在内),此中23个为小分子化学药,16个为医治用生物成品,1个为中成药。
从医治靶点看,石药踊跃规划热点靶点,包含EGFR、DP-1、DPP-4等;在年夜靶点步入红海竞争的环境下,公司开辟临床急需且竞争较小的孤儿药靶点,如ALMB-0166(急性脊髓毁伤);从顺应症看,石药在研1类新药涵盖抗肿瘤、消化体系、心脑血管疾病、本身免疫性疾病、呼吸体系疾病等医治畛域。
石药集团在研的1类新药
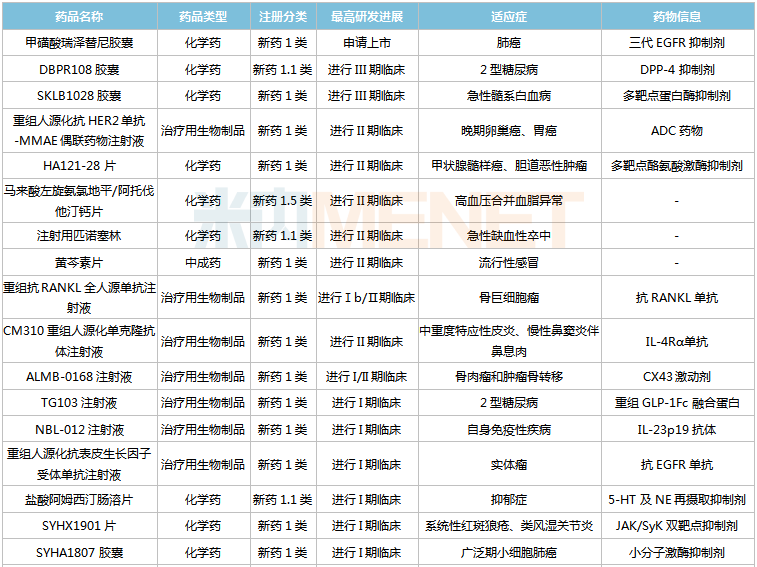
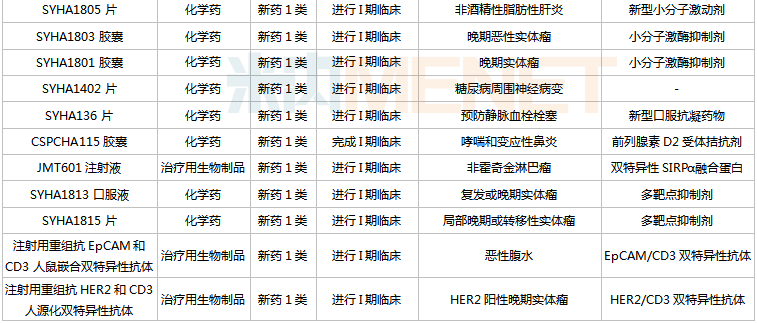
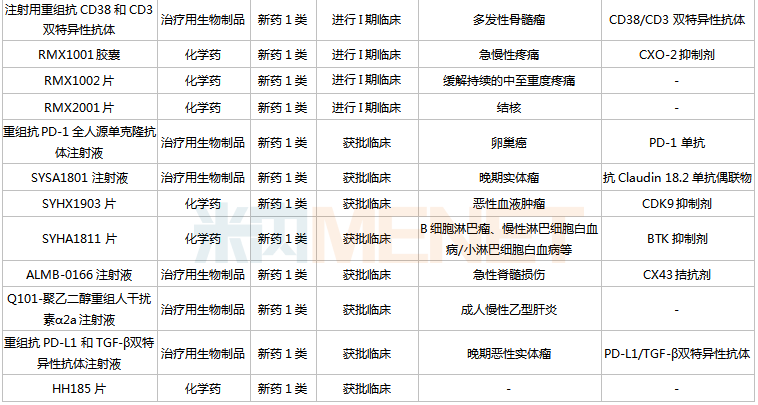
起源:米内网中国药品临床实验公示库
在抗肿瘤畛域,三代EGFR克制剂瑞泽替尼已申请上市,顺应症为肺癌,今朝国际已上市同靶点药物包含豪森的阿美替尼、艾力斯的伏美替尼等;多靶点卵白酶克制剂SKLB1028胶囊正在进行III期临床,实用于FLT3渐变的复发/难治性急性髓系白血病,今朝国际尚无FLT3靶点药物获批;重组人源化抗HER2单抗-MMAE偶联药物打针液(ADC药物)、HA121-28片(多靶点酪氨酸激酶克制剂)、重组抗RANKL全人源单抗打针液(抗RANKL单抗)、ALMB-0168打针液(CX43冲动剂)正在展开II期临床。
在消化体系畛域,DPP-4克制剂DBPR108胶囊正在进行III期临床,用于医治2型糖尿病,同靶点国产新药中,恒瑞的瑞格列汀已报告上市。另一款糖尿病用药TG103打针液(重组GLP-1Fc交融卵白)正在展开I期临床。
在心脑血管畛域,马来酸左旋氨氯地平/阿托伐他汀钙片、打针用匹诺塞林正在展开II期临床,别离用于医治高血压归并血脂异常、急性缺血性卒中;新型口服抗凝药物SYHA136片正在进行I期临床,用于预防静脉血栓栓塞。
在本身免疫性疾病方面,CM310重组人源化单克隆抗体打针液(IL-4Rα单抗)正在展开II期临床,NBL-012打针液(IL-23p19抗体)、SYHX1901片(JAK/SyK双靶点克制剂)正在进行I期临床。
此外,在引进的出口新药方面,5.1类新药度恩西布胶囊已提交上市申请,用于医治滤泡性淋巴瘤,这是一款PI3K-δ/PI3K-γ双重克制剂,国际暂无同靶点药物获批上市。
石药集团在研的部门2类新药
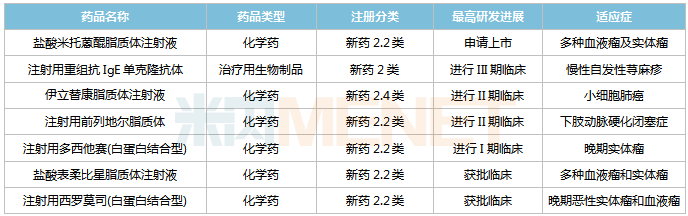
起源:米内网中国药品临床实验公示库
在2类改进型新药方面,石药集团专一于脂质体、纳米等高端制剂,此中盐酸米托蒽醌脂质体打针液已报告上市,伊立替康脂质体打针液、打针用前列地尔脂质体正在展开II期临床;此外,奥马珠单抗生物相似药打针用重组抗IgE单克隆抗体正在展开III期临床,原研产物2020年环球贩卖额超过30亿美元。
56个过评种类19个首家,3个集采种类放量
6月25日,石药集团布告称,集团从属公司石药欧意药业开辟的枸橼酸托法替布片获批临盆并视同过评。米内网数据显示,今朝石药集团已有56个种类通过或视同通过一致性评估,涵盖8个医治年夜类,集中在全身用抗感化药物(20个种类)、消化体系及代谢药(9个种类)及抗肿瘤和免疫调理剂(8个种类)三年夜医治畛域。
石药集团过评环境
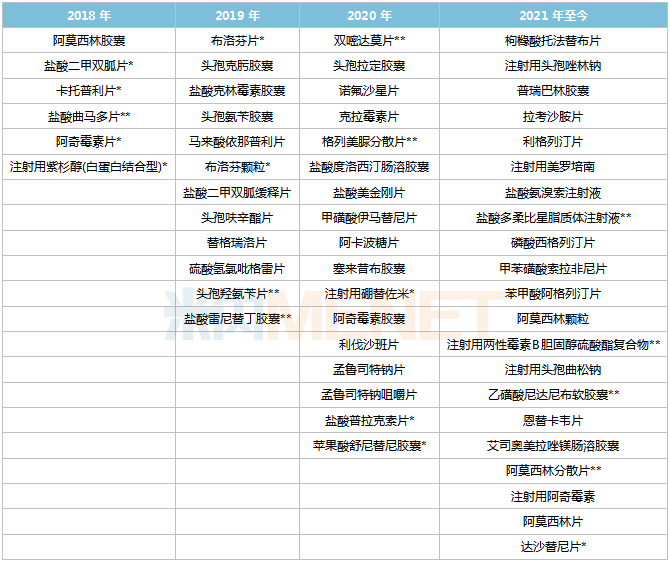
注:带*为首家过评,**为独家过评
起源:米内网MED2.0中国药品审评数据库
19个种类首家过评,盐酸曲马多片、头孢羟氨苄片、盐酸雷尼替丁胶囊、双嘧达莫片、格列美脲疏散片、盐酸多柔比星脂质体打针液、打针用两性霉素B胆固醇硫酸酯复合物、阿莫西林疏散片、乙磺酸尼达尼布软胶囊独家过评。
日前,第五批集采中选成果正式颁布,石药集团有3个种类中选,别离为打针用阿奇霉素、打针用头孢曲松钠及打针用头孢唑林钠。米内网数据显示,石药在上述3款抗感化打针剂所占市场份额均较低。
石药集团第五批集采中选环境(单元:元/瓶)
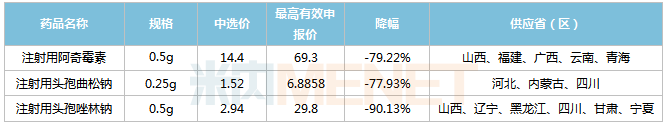
起源:上海阳光医药推销网
11个种类冲刺首仿,5个为独家报告
7月1日,石药欧意药业以仿造4类提交玛巴洛沙韦片上市申请,该产物在国际暂无仿造药获批,原研产物于2021年4月获批出口。米内网数据显示,今朝石药新注册分类报产的仿造药中,有11个暂无首仿获批(含剂型首仿)。
石药已报产且暂无首仿获批的仿造药
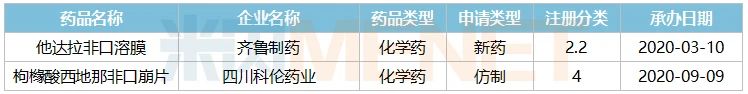
起源:米内网MED2.0中国药品审评数据库
6个种类由石药首家或独家报产,已有8家企业报告的阿普斯特片是一款口服PDE4克制剂,2020年环球贩卖额接近22亿美元;石药独家报产的5个种类中,玛巴洛沙韦片是一款具备新型作用机制的抗流感病毒单剂量口服药物。
起源:米内网数据库,上市公司布告等
注:数据统计截至7月9日,若有疏漏,欢送指正!
医药网新闻
- 相关报道
-
- PNAS:免疫疗法新突破!NOD2基因变异助力癌症治疗 (2025-08-06)
- 《自然· 医学》:按照膳食指南吃可能还不够!最新临床试验显示,即使遵照指南要求吃饭,多吃超加工食品仍会阻碍减重 (2025-08-06)
- 施一公团队发表最新PNAS论文 (2025-08-06)
- 致癌代谢物2HG竟是肥胖“隐形推手”?!Nat Metabol 最新研究中科学家揭秘肥胖发生新机制 (2025-08-05)
- Sci Adv:科学家有望重新训练中性粒细胞来靶向治疗乳腺癌 (2025-08-05)
- 特洛伊木马:复旦大学最新论文登上Cell子刊封面 (2025-08-05)
- TN:南京医科大学团队发现,长期运动可通过改善脑膜淋巴管结构和引流功能,减轻AD病理,并改善小鼠认知功能 (2025-08-05)
- 柳叶刀:塑料危机——对人类从摇篮到坟墓的健康威胁 (2025-08-05)
- Nature子刊:中山大学林浩添/陈崴团队开发AI模型,利用视网膜图像无创诊断慢性肾病 (2025-08-05)
- 四部分脱手!医疗科普不是“流量生意” (2025-08-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















