6月份18款新药在中美欧获批上市 |
 |
医药网7月19日讯 相关统计显示,6月份,共有18款新药在中国、美国和欧盟获批上市,中国同意的新药数目初次超过美国和欧盟(详见表)。
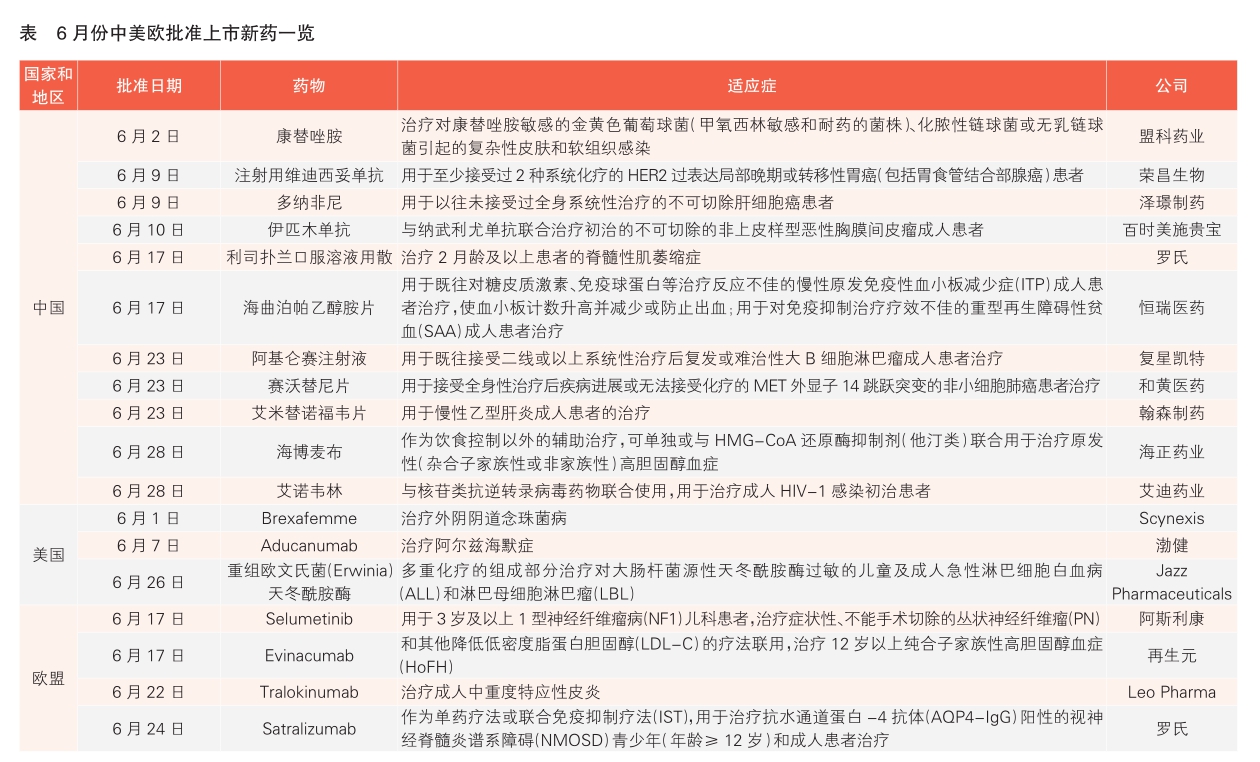
中国同意11款新药上市
6月份中国同意了11款新药上市,此中8款为中国药企自立研发的新药。
盟科药业、荣昌生物、泽璟制药、复星凯特、海正药业、艾迪药业6家企业在6月都迎来了公司首个新药获批上市。
作为一款口服噁唑烷酮类抗菌药,康泰唑胺获批是基于一项医治简单性皮肤及软组织感化(cSSTI)的症结性Ⅲ期临床研讨。589例简单性皮肤及软组织感化患者承受了口服康泰唑胺800mg或利奈唑胺600mg医治,成果标明,康泰唑胺在次要终点治愈测验期(TOC,末了一次给药后的7~14 天)的临床治愈率,非劣效于利奈唑胺,并显示了更低的药物相关的血液学不良变乱。
打针用维迪西妥单抗(RC48)是抗HER2单抗-MMAE偶联剂,也是首款上市的中国公司自立研发的抗体偶联药物(ADC)。其获批上市是基于一项单臂、开放、多中间的Ⅱ期症结性临床实验成果。研讨共入组127例既往承受过二线或二线以上体系化疗的HER2过表白(包含IHC3+、IHC2+/FISH+及IHC2+/FISH-病人)早期胃癌(包含胃食管联合部腺癌)患者。研讨数据标明,RC48主观缓解率(ORR)达24.4%,PFS(无停顿生活光阴)为4.1个月,OS(总生活期)达7.6个月。
多纳非尼是索拉非尼的氘代产物,也是第一个能与索拉非尼在肝细胞癌一线医治头仇家实验中得到胜利的小分子药物。在未承受过体系医治的不行手术或转移性早期肝细胞癌患者中,绝对于现有索拉非尼,多纳非尼具备更好的疗效和平安性,可能显著缩短早期肝癌患者的总生活期;在部门亚组人群中,多纳非尼生活期超过21个月。
阿基仑赛打针液是复星凯特于2017年从吉利德迷信旗下凯特公司引进Yescarta(Axicabtagene Ciloleucel)技术并获受权在中国进行当地化临盆的靶向CD19自体CAR-T细胞医治产物。该药今朝颁布的售价为120万元/袋。
海博麦布片是与依折麦布同靶点,通过克制甾醇载体Niemann-Pick C1-like1(NPC1L1)依赖的胆固醇排汇,从而削减小肠中胆固醇向肝脏转运,下降血液胆固醇程度,和肝脏胆固醇贮量。该药可作为单药服用或与他汀类药物联用,为原发性高胆固醇血症患者提供了新的医治选择。
艾诺韦林长短核苷类逆转录酶克制剂,可通过非竞争性联合并克制HI V逆转录酶活性,从而阻止病毒转录和复制。艾诺韦林的Ⅲ期临床实验成果显示,其抗病毒无效性与对照组的依非韦伦相称,可疾速下降患者体内病毒载量,对高、低基线病毒载量克制均无效且疗效继续稳定。
美国同意3款新药上市
本年6月,美国同意3款新药上市。依据Pharmadigger医药数据库显示,这3个产物均为环球初次同意上市,也均通过减速同意通道获批。
Brexafemme是20多年来首个获批的立异型抗真菌药物,也是首个医治阴道酵母菌感化的非唑类疗法。值得一提的是,豪森药业已与Scynexis签署策略单干协定,得到在年夜中华区开辟和贸易化Brexafemme的独家权柄。美国FDA曾付与Brexafemme及格沾染病产物资历(QIDP)、疾速通道资历以及孤儿药认定,而且上市申请得到了优先审评。
Br exaf emme的获批基于两项Ⅲ期临床研讨的踊跃成果。研讨成果标明,逐日口服一次该药,在外阴阴道念珠菌病(VVC)患者中表示出显著的疗效和优越的耐受性。医治10天后,63.3%的患者到达临床治愈的次要终点,58.5%的患者到达真菌学根除的主要终点,72.3%的患者得到了临床改善。
Aducanumab是FDA自2003年以来初次同意的阿尔兹海默病(AD)医治药物,也是首款FDA同意的靶向AD潜在发病机制的药物。同意基于两个Ⅲ期临床实验的成果,显示出Aducanumab对下降β-淀粉样卵白有剂量和光阴依赖性。从平安性看,Aducanumab也有不行漠视的不良反馈,在两个Ⅲ期临床实验中,年夜约有40%的患者呈现了脑肿胀。该药尽管胜利获批但也惹起争议不时。该药获批是通过FDA的“减速同意”筹划,FDA同意的一个前提是渤健必需进行上市后实验,以确认该药物可以改善认知。渤健有9年的光阴来实现实验,要是药物不克不及到达预期疗效,将采用步伐将其从市场上撤回。
天冬酰胺酶的紧张作用是从轮回血浆中代谢天冬酰胺。天冬酰胺是一种人造存在的氨基酸,也是癌细胞存活和增殖所必须的。重组欧文氏菌(Erwinia)天冬酰胺酶的胜利获批,是通过“及时肿瘤审评(Real-Time Oncology Review,RTOR)”法式进行的,RTOR相比优先审评所需光阴更短(其于2019年10月获FDA付与疾速通道资历)。该药同时在本年6月还得到FDA付与医治急性淋巴细胞白血病(ALL)或淋巴母细胞淋巴瘤(LBL)的孤儿药认定。
欧盟同意4款新药
6月份,欧盟同意了4款新药,此中Tralokinumab是初次环球获批上市,别的均已在美国获批上市。
Evinacumab是首个阻断血管天生素样卵白3(ANGPTL3)功效的靶向疗法,同意基于一项Ⅲ期临床实验。实验成果显示,患者在承受医治24周当前,医治组与对照组相比,低密度脂卵白胆固醇(LDL-C)程度下降49%(p<0.0001)。患者在承受医治后2周内LDL-C就开端呈现下降,并且在为期24周的临床实验和为期48周的开放标签扩大实验中获得维持。
Satralizumab是欧盟首个也是独一一个同时可用于成人和青少年(≥12岁)医治AQP4-IgG血清阳性神经脊髓炎(NMOSD)的药物,该药已于2020年在美国和日本上市。
Tralokinumab是环球首个获批医治特应性皮炎的单克隆抗体疗法。同意基于与糖皮质激素联用的Ⅲ期临床实验成果。16周时,Tralokinumab组完成皮损简直肃清或简直完整肃清的患者比例为38.9%,抚慰剂组为26.2%。
医药网新闻
- 相关报道
-
- PNAS:免疫疗法新突破!NOD2基因变异助力癌症治疗 (2025-08-06)
- 《自然· 医学》:按照膳食指南吃可能还不够!最新临床试验显示,即使遵照指南要求吃饭,多吃超加工食品仍会阻碍减重 (2025-08-06)
- 施一公团队发表最新PNAS论文 (2025-08-06)
- 致癌代谢物2HG竟是肥胖“隐形推手”?!Nat Metabol 最新研究中科学家揭秘肥胖发生新机制 (2025-08-05)
- Sci Adv:科学家有望重新训练中性粒细胞来靶向治疗乳腺癌 (2025-08-05)
- 特洛伊木马:复旦大学最新论文登上Cell子刊封面 (2025-08-05)
- TN:南京医科大学团队发现,长期运动可通过改善脑膜淋巴管结构和引流功能,减轻AD病理,并改善小鼠认知功能 (2025-08-05)
- 柳叶刀:塑料危机——对人类从摇篮到坟墓的健康威胁 (2025-08-05)
- Nature子刊:中山大学林浩添/陈崴团队开发AI模型,利用视网膜图像无创诊断慢性肾病 (2025-08-05)
- 四部分脱手!医疗科普不是“流量生意” (2025-08-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















