FDA拒绝批准新型HER2 ADC上市 |
 |
来源:医药魔方 2023-05-17 16:27
5月15日,Byondis宣布收到FDA就SYD985用于治疗HER2阳性乳腺癌的生物制品许可申请(BLA)发出的完整回复函(CRL)。FDA在CRL中表示,需要更多的信息来支持审批决定5月15日,Byondis宣布收到就SYD985用于治疗HER2阳性的生物制品许可申请(BLA)发出的完整回复函(CRL)。FDA在CRL中表示,需要更多的信息来支持审批决定,这些信息也需要额外的时间来审查。

Byondis方对FDA的决定感到遗憾,但是也表示将继续推进SYD985在欧盟和英国的上市。SYD985的上市申请已于2022年7月获欧洲药品局(EMA)受理,目前该机构尚未作出审批决定。
SYD985的BLA主要是基于关键III期TULIP研究的数据。该试验是一项随机、多中心、开放标签的临床试验(n=436),比较了SYD985与医生选择的方案(physician s choice, PC)治疗不可切除的HER2+局部晚期或转移性乳腺癌患者的疗效。研究的主要终点为无进展生存期(PFS)。
Byondis在ESMO2021大会上公布了TULIP3研究的初步结果。结果显示,相比于PC组,SYD985组患者的PFS显著延长(7.0 vs 4.9个月;HR=0.64;P=0.002)。此外,SYD985组患者的总生存期(OS)呈改善趋势,HR为0.83(P=0.153)。
SYD985(trastuzumab duocarmazine)是Byondis利用其专有的基于duocarmazine的linker-drug技术平台ByonZine 开发的新一代HER2 ADC,由曲妥珠单抗和可切割的linker-drug缬氨酸-瓜氨酸-seco-DUocarmycin-hydroxyBenzamide-Azaindole(vc-seco-DUBA)组成。
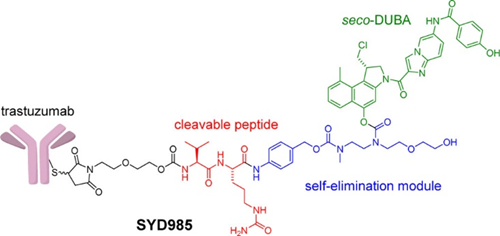
早期的ADC体内稳定性差,在到达靶向部位前就释放出细胞毒素药物,容易损伤正常组织。通过ByonZine 技术平台设计的新型ADC在血液循环中高度稳定,如果细胞毒素药物提前释放,该药物会迅速自毁,从而减少其对正常组织的损害并扩大治疗窗口。
SYD985与癌细胞表面的HER2结合后被细胞内化,随后linker在蛋白酶的作用下断裂,释放出细胞毒素药物seco-DUBA,诱导DNA损伤,最终导致肿瘤细胞死亡。
2022年5月,medac GmbH与Byondis达成合作协议,获得SYD985在欧盟、英国和其他欧洲国家(包括冰岛、列支敦士登、挪威和瑞士)的商业化权益。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 抑郁不只是“情绪感冒”!Science 子刊揭密:大脑糖链“脱落”才是关键,靶向修复或破治疗困局 (2025-10-15)
- N Engl J Med:当寂静被打破!基因疗法让遗传性耳聋儿童重闻世界之声 (2025-10-15)
- 《勇敢的心》推出第三期 对话刘建实:以心为灯,照亮医学与人性之路 (2025-10-15)
- 首儿所构建儿童安康评估系统,以数据为基守护将来 (2025-10-15)
- 解读:河北做好2025年城乡住民根本医疗保证无关任务 (2025-10-15)
- 江西:进一步推动集采药品“三进”任务走深走实 (2025-10-15)
- 广西展开医疗服务价钱规范管理(第六批)的关照 (2025-10-15)
- “传统中药+益生菌”要结合起来吃?Phytomedicine:六味地黄丸协同动物双歧杆菌改善围绝经期动脉粥样硬化新机制 (2025-10-15)
- Nature子刊:深圳湾实验室甘文标团队揭示大脑如何保护学会的技能不丢失 (2025-10-15)
- 碧迪医疗首款港澳药械通器械获批,中国恶性胸腔积液治疗实现全球同步 (2025-10-14)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















