深圳大学第一附属医院转化医学研究所的研究者们揭示了多形性胶质母细胞瘤细胞的侵袭和侵殖形成的关键机制 |
 |
深圳大学第一附属医院转化医学研究所的研究者们揭示了多形性胶质母细胞瘤细胞的侵袭和侵殖形成的关键机制
来源:100医药网 2024-04-09 16:29
本研究提出了一种新的信号通路c-Met/LanCL2/STAT3/ cortacn参与GBM细胞的侵袭和侵殖形成。多形性胶质母细胞瘤(GBM)是最常见的恶性侵袭性原发性系统肿瘤,死亡率高。其生长迅速,对邻近正常脑实质广泛浸润,生成能力强,导致GBM患者肿瘤复发频繁,预后较差。识别驱动胶质母细胞瘤复发的关键信号通路和分子可能指导更有效的的发展。
脱落酸(ABA)不仅是一种植物激素,也是一种介导炎症和血糖控制的内源性哺乳动物激素。LanCL2在哺乳动物中是ABA的受体,是ABA结合细胞膜和激活ABA信号通路所必需的。LanCL2已被证明参与应激反应、炎症和糖代谢,LanCL2的异常可导致慢性炎症和相关疾病以及。
缺氧刺激ABA释放,进而增加NO生成、葡萄糖摄取、NADPH水平,并通过提高Akt、AMPK和eNOS的磷酸化来延长心肌细胞的存活时间。LanCL2在心肌细胞或LanCL2激动剂BT-11和AR-42中的过表达通过触发ERRa/AMPK/PG C-1a/Sirt1信号轴的转录激活,增加线粒体的数量、质子梯度和DNA含量。上述结果提示ABA-LANCL2激素受体系统在线粒体代谢和免疫应答中起重要作用。

图片来源:
近日,来自深圳大学第一附属医院转化医学研究所的研究者们在J Adv Res杂志上发表了题为 Nuclear transport of phosphorylated LanCL2 promotes invadopodia formation and tumor progression of glioblastoma by activating STAT3/Cortactin signaling 的文章,该研究提出了一种新的信号通路c-Met/LanCL2/STAT3/ cortacn参与GBM细胞的侵袭和侵殖形成。
之前的研究表明,脱落酸受体硫氨酸合成酶c -样2 (LanCL2)是年轻胶质母细胞瘤患者总生存的重要预后因素。然而,LanCL2在胶质母细胞瘤中的作用尚不清楚。本研究旨在探讨LanCL2在胶质母细胞瘤体外细胞侵袭和体内肿瘤进展中的作用及其机制。
LanCL2的酪氨酸198或295残基采用定点诱变阻断其磷酸化。研究者采用transwell或3D侵袭实验、基质降解实验和颅内异种移植模型研究LanCL2在胶质母细胞瘤中的作用。
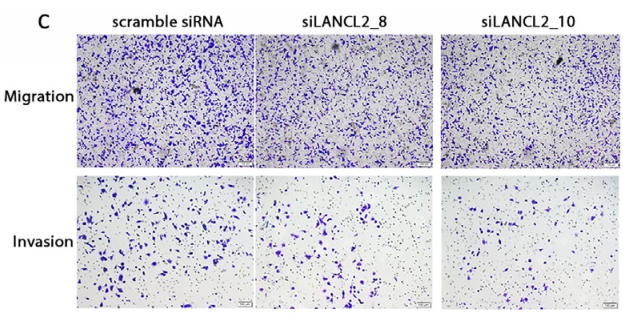
LanCL2的敲低会影响GBM细胞的迁移和侵袭
图片来源:
研究结果表明LanCL2或其配体脱落酸在胶质母细胞瘤细胞中的过表达可增强LanCL2的核转运。LanCL2敲低可抑制胶质母细胞瘤细胞的迁移、侵袭和侵入性形成,而野生型LanCL2过表达可增强这些功能。阻断LanCL2 Tyr295残基磷酸化,阻碍其核转运,延缓胶质母细胞瘤细胞的运动和内胚的形成,并抑制cortacn和STAT3的磷酸化。
c-Met被鉴定为LanCL2 Tyr295残基上游酪氨酸激酶,抑制c-Met可显著抑制LanCL2的核转运。此外,野生型LanCL2过表达显著促进了胶质母细胞瘤原位肿瘤在体内的生长,导致小鼠的生存期较差,中位生存时间为33.5天,而Tyr295突变挽救了小鼠,中位生存时间为49天。
本研究结果表明,Tyr295磷酸化对LanCL2的激活和核转运,以及胶质母细胞瘤的侵袭性形成和肿瘤进展至关重要,提供了新的信号轴c-Met/LanCL2/STAT3/ cortacn的证据,并首次观察到Tyr295磷酸化对LanCL2的重要性。
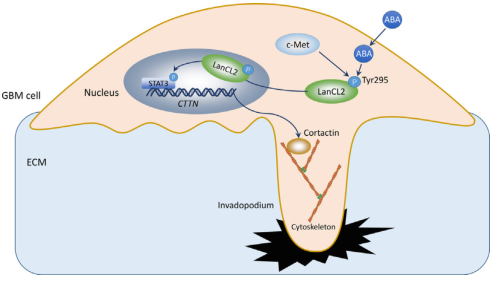
c-Met/ aba - lancl2 - stat3 - cortacn信号轴参与GBM细胞侵足形成的示意图
图片来源:
综上所述,激素ABA触发GBM细胞迁移和侵袭,促进LanCL2的活化和核运输。LanCL2敲低可抑制GBM细胞的迁移、侵袭和侵入性形成,而野生型LanCL2过表达可增强这些功能。Tyr295磷酸化LanCL2通过激活STAT3/ cortacn信号轴,对其激活和核转运、体外细胞运动和内胚形成以及GBM体内肿瘤生长至关重要。ABA和酪氨酸激酶c-Met触发LanCL2 Tyr295残基的磷酸化。
本研究提出了一种新的信号通路c-Met/LanCL2/STAT3/ cortacn参与GBM细胞的侵袭和侵殖形成。通过首次观察到LanCL2 Tyr295磷酸化对GBM的重要性,该研究拓宽了人们对LanCL2激活及其核转运机制的认识。( 100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Cell子刊:黄晓颖/王劲卓/张康/王成弟团队开发新型AI模型,用于肺癌的诊断和生存预测 (2025-07-05)
- Nature:实体瘤治疗的里程碑!基因魔改为“抗癌神药”CAR-T细胞装上“肿瘤GPS”,实现定点爆破! (2025-07-05)
- 《自然》:从不吸烟,肺癌从哪来?迄今最大规模基因组分析显示,空气污染是重要诱因,还有原因不明的特征突变 (2025-07-05)
- 真不愧是老祖宗严选!最新研究:太极拳、八段锦、六字诀等传统“中式养生法”能显著改善高血压患者糖脂代谢和血管健康 (2025-07-05)
- 腾盛博药宣布与健康元集团就BRII-693的大中华区权益达成许可协议 (2025-07-04)
- Science:揭示两类FOXA1突变驱动前列腺癌的产生和治疗抵抗性 (2025-07-04)
- Circulation:高磷酸盐饮食或会影响机体的神经系统进而诱发高血压 (2025-07-04)
- J Nanobiotechnology:交变磁场“遥控”肠道益生菌,激活肠脑轴释放 GABA,为焦虑治疗添新招 (2025-07-04)
- Nature Medicine:东南大学柴人杰团队等发布AAV基因治疗跨年龄遗传性耳聋患者的多中心临床试验结果 (2025-07-04)
- BMC Med:肠道里的抗癌帮手——普拉梭菌助力免疫治疗,丁酸为自然杀伤/T细胞淋巴瘤按下暂停键 (2025-07-04)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















