Cell:利用靶向RNA的CRISPR/Cas13成功鉴定出对人体细胞至关重要的长链非编码RNA |
 |
来源:100医药网 2024-11-29 10:52
作者发现了778种对细胞功能至关重要的lncRNA,包括46种普遍至关重要的核心lncRNA和732种对某些细胞类型具有特异功能的lncRNA。基因包含制造蛋白的指令,生物学的中心法则是这些信息从 DNA 流向 RNA,再流向蛋白。但是,人类基因组中只有 2% 真正编码蛋白;其余 98% 的功能在很大程度上仍然未知。人类遗传学面临的一个紧迫问题是了解这些基因组区域的功能。历史上,有些人甚至把这些区域称为 垃圾 。
如今,在一项新的研究中,来自纽约大学和纽约基因组中心的研究人员发现一些非编码 RNA 其实并不是垃圾 它们具有功能性,在人体的细胞中发挥着重要作用,包括在癌症和人类发育过程中。相关研究结果于2024年11月11日在线发表在Cell期刊上,论文标题为 Multiscale organization of neuronal activity unifies scale-dependent theories of brain function 。

作者利用靶向 RNA 而不是 DNA 的 CRISPR 技术,在整个基因组中进行了搜索,发现了近 800 种对来自不同组织的多种人类细胞的功能非常重要的非编码 RNA。
论文通讯作者、纽约大学生物学副教授Neville Sanjana说, 这项对功能性非编码 RNA 的调查推进了我们对人类基因组的了解,并展示了 CRISPR 筛选的潜力,它可以特异性地靶向 RNA,甚至是那些不编码蛋白的 RNA。
更精确靶向RNA的 CRISPR
基因编辑技术CRISPR给生物医学研究带来了革命性的变化,它的应用非常广泛,从提高农作物产量到通过编辑人血细胞中的DNA来治疗血液疾病。
大多数 CRISPR 应用都使用一种名为 Cas9 的酶在 DNA 水平上编辑基因。然而,一种更新的技术利用Cas13酶更精确地靶向RNA,而不会破坏附近的蛋白编码基因和其他调控元件。
Sanjana实验室之前展示了如何优化靶向RNA而不是DNA的CRISPR-Cas13平台,以筛选整个转录组。
许多研究已利用测序技术读出了哪些RNA被表达,但要了解特定的RNA分子是否真地是细胞功能所必需的,一直是个挑战。
论文共同第一作者、Sanjana实验室博士后Simon M ller问道, 我们如今拥有了这项技术,但生物学问题依然存在:非编码基因组的哪些部分实际上具有功能?
毕竟不是垃圾
利用CRISPR-Cas13编辑RNA并避免脱靶活性,作者系统分析了5种人类细胞系(包括、和细胞)中近6200对长链非编码RNA(lncRNA)基因和附近的蛋白编码基因。
他们利用CRISPR扰乱或敲除每个lncRNA,看看会发生什么 细胞是会死亡、停止增殖,还是可以耐受?并确定每个lncRNA是否是必需的。
论文共同第一作者、Sanjana实验室博士后Wen-Wei Liang说, 有了Cas13,我们可以具体地询问 这些转录本的功能是什么? 它们不是垃圾,我们发现它们对细胞的生长和分裂确实非常重要,而且是必不可少的。
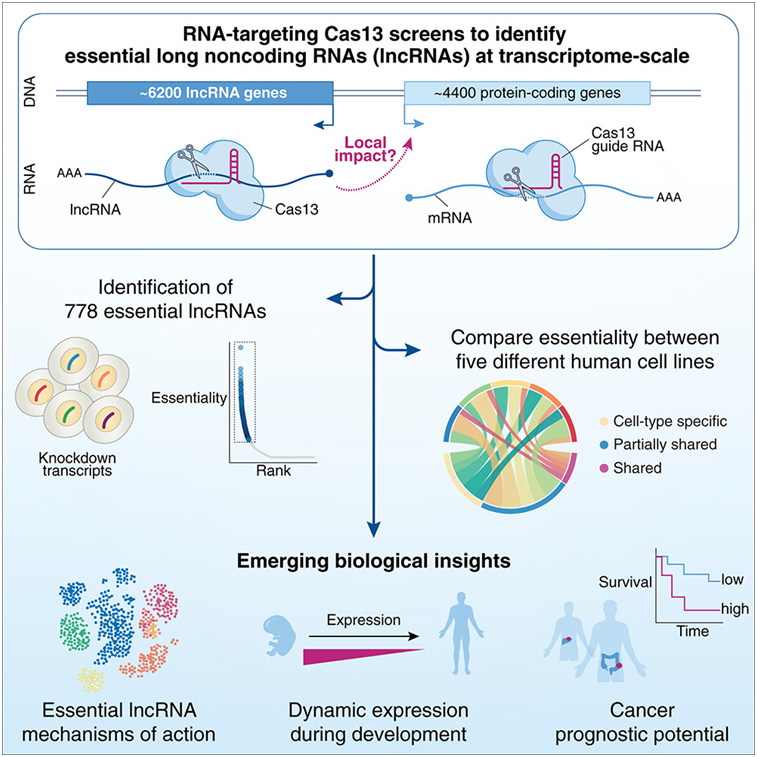
利用靶向RNA的Cas13筛选在转录组水平上确定必需的lncRNA
作者发现了778种对细胞功能至关重要的lncRNA,包括46种普遍至关重要的核心lncRNA和732种对某些细胞类型具有特异功能的lncRNA。他们随后将这些必需的lncRNA与蛋白编码基因进行了比较。就蛋白编码基因而言,如果一个基因在五种细胞系中的一种中是必需的,那么它在其他细胞系中也很可能是必需的。相比之下,必需的lncRNA更具有细胞类型特异性。
作者很想知道,必需的 lncRNA 是否会调节附近的蛋白编码基因,这个机制上的问题从未针对非编码 RNA 进行过研究。在这项研究中,他们发现绝大多数必需的lncRNA都是独立于附近的蛋白编码基因运行的。
他们还发现必需的lncRNA会调节细胞增殖的关键通路 这一过程在人类发育和癌症中都很重要,它们的缺失会影响细胞的发育并导致细胞死亡。
值得注意的是,许多重要的lncRNA在人类发育早期的组织中表达量很高,而在后期则表达量较低,这表明某些lncRNA在发育过程中发挥着重要作用。
此外,在对大约9000份肿瘤样本的分析中,作者发现了在特定类型肿瘤中的表达发生改变的lncRNA,并精确定位了那些在肿瘤中的表达与不同癌症中生存率的好坏有关的lncRNA。
Sanjana补充说, 这些非编码RNA可能会产生新的生物标志物和癌症治疗靶点,鉴于它们的细胞类型特异性表达,这是个性化医疗的一个潜在机会。 (100yiyao.com)
参考资料:
Wen-Wei Liang et al. . Cell, 2024, doi:10.1016/j.cell.2024.10.021.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:揭示小细胞肺癌劫持神经元突触从而加速生长背后的分子机制 (2025-09-12)
- Nat Commun:口腔微生物界的“超级英雄”!科学家揭示细胞外遗传元素Inocle的发现与意义 (2025-09-12)
- Trends Biotechnol.:武汉大学陈刚/余自力等团队提出FACTORY全自动 EV 分离平台,把 EV 分离从“小作坊”直接升级成“标准化工厂” (2025-09-12)
- EMBO Mol Med:罕见基因突变有望揭示肠道干细胞的再生奥秘 (2025-09-11)
- STTT:打断肿瘤的“狗腿”!科学家发现,抑制中性粒细胞的STAT3,会让中性粒细胞“改邪归正”,促进T细胞抗癌 (2025-09-11)
- Cell:IL-25诱导的记忆2型固有淋巴细胞,强化黏膜免疫 (2025-09-11)
- Nature Medicine:靶向休眠肿瘤细胞,预防乳腺癌复发 (2025-09-11)
- PLoS Biol:肠道真菌与人类健康——科学家揭秘基因与微生物的神秘联系! (2025-09-11)
- Nature重磅:“装甲型”CAR-T治疗实体瘤新突破,细胞因子精准“爆破”且全身毒性归零 (2025-09-11)
- 【9·10致敬全体教师】2025细胞外囊泡大会(厦门站)免费票速抢!! (2025-09-10)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















