iPS细胞技术新成果!Biomaterials:二维培养肝类器官,解锁药物研发新“肝”线 |
 |
来源:100医药网 2025-02-08 09:06
本研究成功建立人诱导多能干细胞来源的肝类器官,优化培养条件使其高效增殖且高表达肝基因;开发二维培养法获得功能强大的肝细胞,其具备多种肝功能、高药物代谢酶活性且对肝毒性药物有响应。
在医药研发领域,肝细胞模型的选择对药物代谢和毒性评估起着关键作用。原代人肝细胞(PHHs)虽被视为金标准,但它在体外无法增殖,且功能易衰退。人诱导多能(iPS)来源的肝细胞样细胞(HLCs)虽有潜力,却存在功能弱、分化时间长和难以大量制备的问题。
近日,一项发表于Biomaterials的研究Two-dimensionally cultured functional hepatocytes generated from human induced pluripotent stem cell-derived hepatic organoids for pharmaceutical research带来了新的解决方案。该研究利用人iPS细胞来源的肝类器官(iHOs),通过优化培养条件和开发二维(2D)培养方案,获得了功能强大的iHO-Heps肝细胞,有望在药物研发中发挥重要作用。

研究人员在建立和培养iHOs时,对不同培养基进行了筛选。结果发现,Hep-Medium培养基更适合iHOs的生长。在Hep-Medium培养基中,iHOs在18天内可增殖约105倍,比Chol-Medium培养基快100倍。同时,Hep-Medium培养基能显著提高iHOs中大多数肝细胞标记基因的表达水平,且这种效果至少能维持到第10代。此外,研究还表明,从终末分化(第25天)的HLCs建立的iHOs,最适合生成具有更高肝功能的肝细胞。
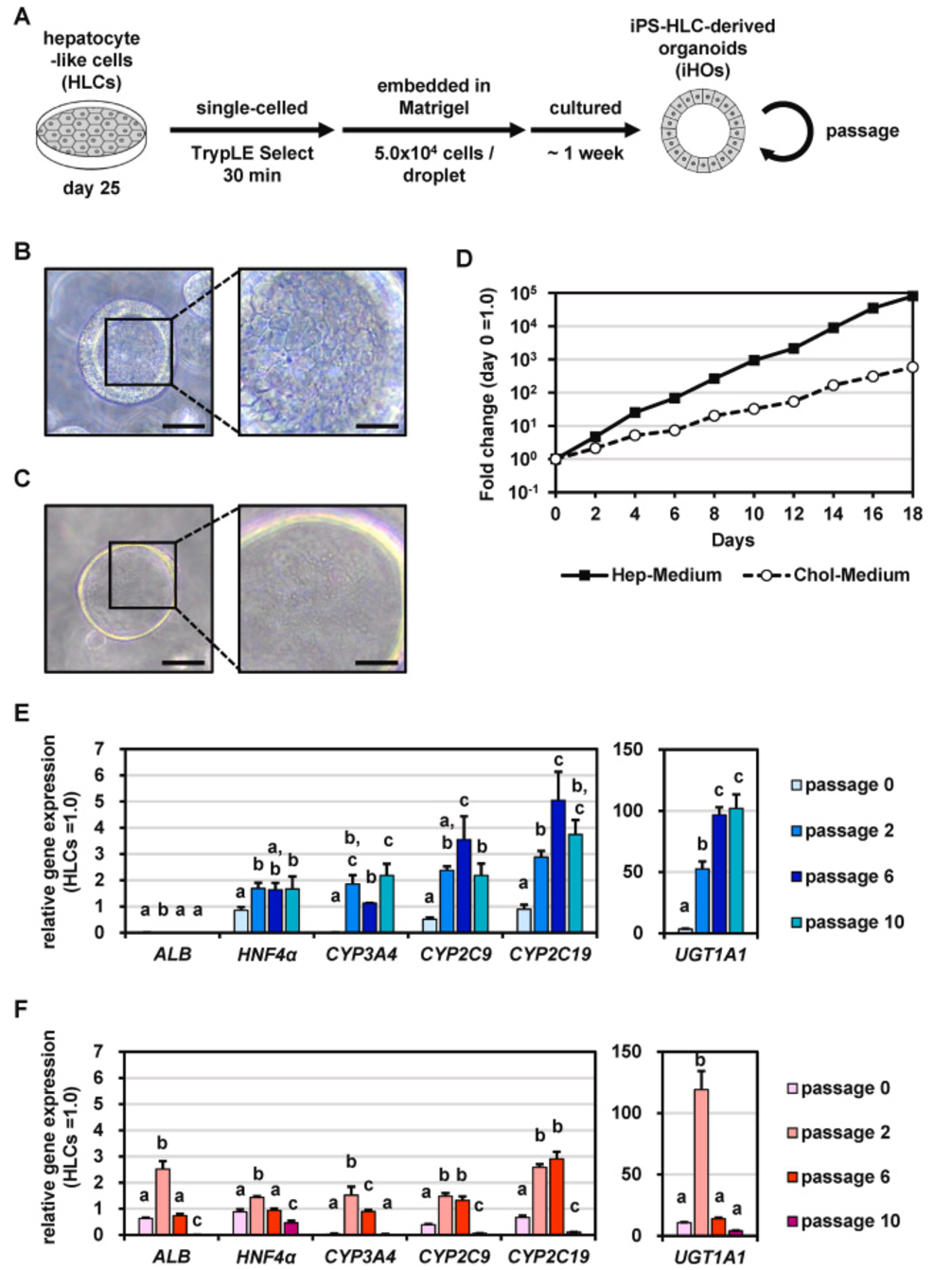
图 1. 肝类器官建立和培养的适宜培养基
为使iHOs更广泛地应用于药物研发,研究人员对其进行了2D培养。经过11天的逐步培养,添加多种生长因子和化学物质,得到的iHO-Heps呈现出典型的肝细胞多边形形态。iHO-Heps的肝基因表达和CYP3A4活性显著高于在Hep-Medium或Diff-Medium中培养的细胞。与HLCs、iHOs和PHHs相比,iHO-Heps中HNF4 和CYP酶等基因的表达水平相当或更高,即使iHOs传代15次后,仍能产生高功能的2D肝细胞。而且,iHO-Heps中钠牛磺胆酸共转运多肽(NTCP)基因表达恢复,白蛋白(ALB)基因表达也有所恢复,虽然仍低于HLCs,但已显示出良好的应用潜力。
在评估iHO-Heps的肝功能时,发现其具备多项重要功能。iHO-Heps能进行糖原储存,可有效摄取和释放吲哚菁绿(ICG),还能分泌白蛋白和尿素。此外,通过特定培养和检测方法,证实了iHO-Heps具有形成胆小管的能力。进一步研究发现,从第25天分化细胞建立的iHO-Heps,在CYP3A4活性、白蛋白分泌和尿素分泌等方面表现最佳。
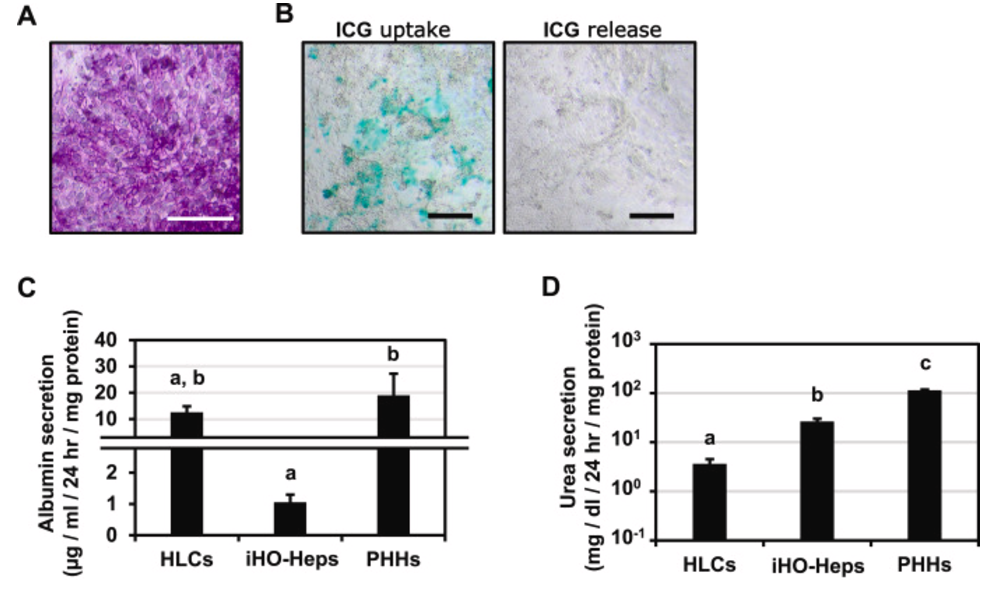
图 2. iHO-Heps的肝功能
在药物代谢和响应能力方面,iHO-Heps表现出色。与HLCs相比,iHO-Heps的多种CYP酶活性大幅提高,其中CYP3A4和CYP2C19的活性比PHHs还高。在对肝毒性药物的响应实验中,iHO-Heps与PHHs对不同药物的敏感性相似,表明iHO-Heps可用于研究多种药物的代谢和响应。

图 3. iHO-Heps的药物代谢能力和药物反应性
RNA-seq分析显示,iHOs的建立激活了细胞增殖相关通路,而2D培养则使细胞从增殖状态转变为代谢状态,激活了药物代谢等相关通路。
总体而言,这项研究成功克服了HLCs的局限性,建立了优化的iHOs培养方案,通过2D培养获得的iHO-Heps具备多种关键肝功能和强大的药物代谢能力。这一成果为药物研发提供了更可靠的肝细胞模型,有助于更准确地评估药物代谢和毒性。同时,也为研究肝脏疾病发病机制和个性化药物治疗提供了新的工具。尽管目前仍有进一步优化的空间,但该研究无疑为医药研发领域带来了重要突破,有望推动未来医药研究的快速发展。(100yiyao.com)
参考文献:
Inui J, Ueyama-Toba Y, Imamura C, Nagai W, Asano R, Mizuguchi H. Two-dimensionally cultured functional hepatocytes generated from human induced pluripotent stem cell-derived hepatic organoids for pharmaceutical research.Biomaterials. Published online January 28, 2025. doi:10.1016/j.biomaterials.2025.123148
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 11家创新药公司完成新一轮融资! (2025-09-25)
- 自闭症社交障碍有破解之法?Nat Commun:大脑里的“社交激素”通路断了,激活受体就能修复 (2025-09-25)
- 不分时间“秒睡”,警惕这种被忽视的病!全球数十款新药加速冲刺,正在为患者点亮希望 (2025-09-25)
- 每月吃 1 片就能防 HIV ?PLoS Biol:一种新型HIV抗逆转录病毒口服药来了,长效还抗耐药 (2025-09-25)
- 益生菌来源 EVs 攻克脂肪肝!Front Immunol:无需活菌定植的“益生菌精华”,降肝酶、稳血脂还护肠道 (2025-09-25)
- 《自然》子刊:鼻腔菌群也能影响大脑!上海交大/上科大团队发现,鼻腔金黄色葡萄球菌通过降解性激素介导抑郁行为 (2025-09-25)
- 老药新用!黄波团队发现碳酸锂可逆转肺纤维化,清除“瘢痕制造者”肌成纤维细胞 (2025-09-25)
- Cell:一种保护性涂层有望让通用型CAR-T细胞疗法成为可能 (2025-09-25)
- 原来植物也有“疗伤因子”!ACS Appl Mater Interfaces:丹参来源囊泡,让受损神经在大鼠身上“重连” (2025-09-25)
- 精鼎医药宣布任命 Rob Goodwin 担任公司首席运营官 (2025-09-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















