NEJM:又见CAR脱轨!科学家首次发现,CAR会插入并抑制抑癌基因TP53表达,或驱动继发T细胞淋巴瘤 |
 |
NEJM:又见CAR脱轨!科学家首次发现,CAR会插入并抑制抑癌基因TP53表达,或驱动继发T细胞淋巴瘤
来源:奇点糕 2025-02-08 11:00
虽然Mailankody团队只报道了一个病例的分析数据,但是它为插入突变是CAR-T细胞治疗后继发T细胞淋巴瘤的诱因,提供了支撑。当年5月底,美国宾夕法尼亚大学J. Joseph Melenhorst和Carl H. June领衔的团队,在《自然》上发表了一篇研究论文[1]。他们意外发现,在改造T细胞的时候,CAR被无意插到TET2基因里,造成该基因功能障碍。然而,患者却 因祸得福 ,因为注入患者体内的这种细胞增殖能力更强、抗癌能力更强、活得也更久,最终患者也因此实现了临床治愈。
不过,意外往往充满了不确定性,有好的一面,就会出现坏的一面。仅仅4个月之后,Melenhorst和June团队又在《自然 医学》上发表了一篇让人震惊的研究论文[2]。这一次,在制作CAR-T细胞时,意外地将CAR整合到癌细胞基因组中,形成了 CAR-癌细胞 ,导致患者最终因癌症复发而死亡。
近日,由纪念斯隆-凯特琳癌症中心Sham Mailankody领衔的研究团队,在顶级医学期刊《新英格兰医学杂志》发表了一个罕见的病例报道[3]。他们在一例接受CAR-T治疗后继发CD4阳性T细胞的患者肿瘤组织中,首次发现了CAR整合到T细胞抑癌基因TP53中的现象,并推测这个现象是继发T的驱动因素之一。

▲论文首页截图
研究报道的是一名72岁女性患者,她因患难治性/复发性,接受了自体BCMA特异性CAR-T细胞(ciltacabtagene autoleucel)治疗。患者在输注CAR-T细胞的一个月之后,实现了微小残留病灶(MRD)阴性的完全缓解。
然而,在CAR-T细胞输注约2个月之后,患者却出现了持续恶心、呕吐、厌食和难治性水样非血性腹泻,最终住院治疗。不过,患者没有发现感染的迹象,腹部和盆腔的CT扫描也未发现任何临床上明显的异常;上消化道内镜和柔性乙状结肠镜检查,在食道、胃、近端和整个结肠中也没有发现明显异常(两次检查均获得了活检样本)。
组织活检的结果显示,可能是一种不明原因的介导的小肠结肠炎。因此,患者又接受了多种治疗方案的治疗。在治疗后,患者的食欲有所改善,腹泻次数也减少了,甚至有望出院;然而,在出院前不久,患者出现败血症,最终因此死亡。
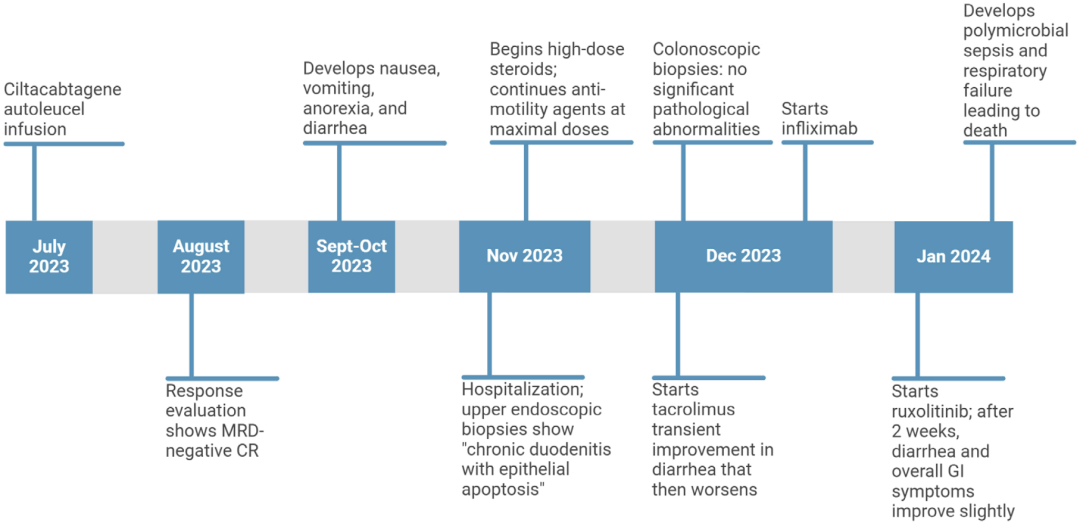
▲患者就医历程
也就是说,医生并不知道患者的真正死因。不久之后,医院里搭建了检测样本中ciltacabtagene autoleucel的CAR构建体的液滴式数字PCR平台,研究人员又借助于这个平台,从患者的十二指肠活检样本中检测到了高丰度的CAR。
这一发现引起了Mailankody团队的注意。于是,他们又重新启动了病理检测。检测结果显示,患者的死因可能是消化道惰性CD4阳性T细胞淋巴瘤或淋巴增生性疾病。在分析TCR序列之后,发现TCR V 11-02克隆占到了83.59%。值得注意的是,这个克隆在CAR-T细胞输注之前不存在,在输注之后,在外周血中的占比从第28天的0.01%,发展到第74天的16.99%。不难看出,这个CAR-T细胞克隆在患者体内大量扩增。
在分析CAR在T细胞基因组中插入位点时,发现了两个显性位点:一个是TP53基因的第一个内含子,插入频率为29%;另一个是TANGO2基因的第一个内含子,插入频率为23%。TP53我们都熟悉,是大名鼎鼎的抑癌基因,在检测组织样本中p53表达情况时,研究人员也发现,约90%的T细胞p53蛋白表达较弱或不表达;而TANGO2虽然也有CAR插入,但是转录和表达没有受到影响,此外,也没有研究发现它与癌症有关。
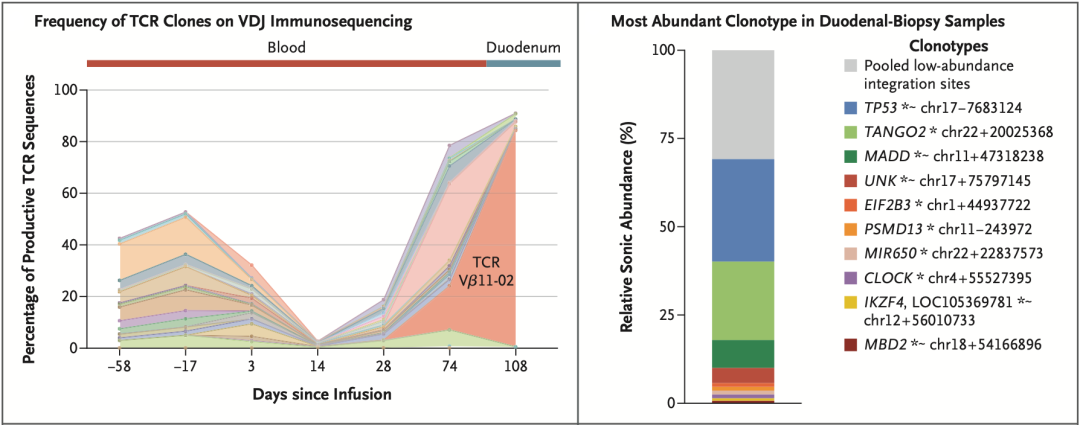
▲分子检测结果
很显然,CAR插入到TP53基因中,抑制了抑癌基因的表达,可能就是驱动T细胞淋巴瘤的关键原因。不过,Mailankody团队在分析58名接受CD19靶向CAR-T细胞治疗的患者数据之后,也在TP53基因中发现了19个独特的整合位点,但没有一个与T细胞的克隆扩增相关,这表明仅TP53的单等位基因整合,可能不足以将CAR-T转化为恶性细胞。
于是,Mailankody团队又分析了T细胞中的基因突变情况,发现JAK-STAT通路的负调控因子SOCS1(抑癌因子)的S206F突变,随着输注时间的推移,逐渐增加,且在时间上与TCR V 11-02克隆相吻合。此外,免疫组化分析也证实JAK-STAT通路被激活,而且这名患者在使用JAK2抑制剂芦可替尼(ruxolitinib)治疗后,继发的临床症状明显好转。
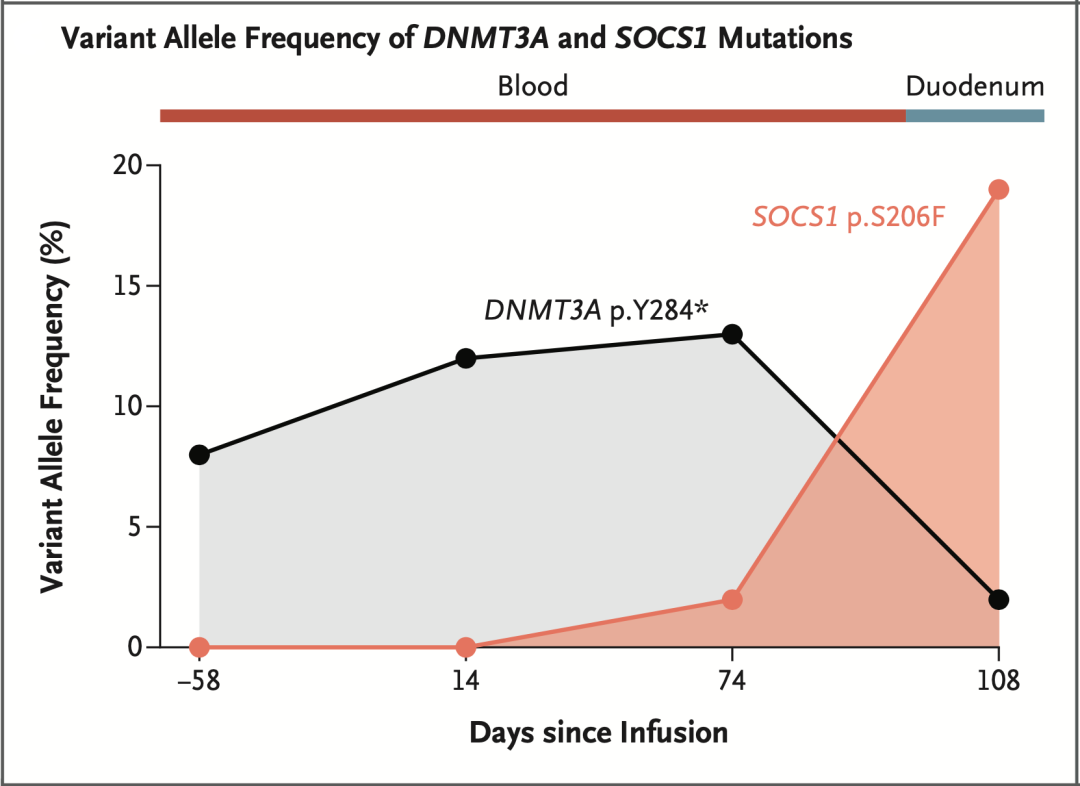
▲SOCS1突变浮出水面
基于以上研究数据,Mailankody团队认为,对于这位患者而言,CAR-T细胞输注后可检测到的SOCS1基因突变,以及CAR与TP53基因的整合,可能共同导致了CAR-T治疗后继发的CAR阳性T细胞淋巴瘤的发生。
我们稍微理一下推理逻辑:CAR插入TP53基因,导致这个抑癌基因表达下调,赋予了CAR-T细胞恶变的潜能;而SOCS1基因突变,会激活JAK-STAT信号通路,进一步推动CAR-T细胞恶性转化;最终表现就是TCR V 11-02克隆飙升,导致患者死亡。当然,背后的分子机制,还有待进一步研究证实。
总的来说,虽然Mailankody团队只报道了一个病例的分析数据,但是它为插入突变是CAR-T细胞治疗后继发T细胞淋巴瘤的诱因,提供了支撑。更重要的是,它也提醒临床研究人员,要进一步优化CAR的整合方式,并做好CAR-T细胞疗法的长期安全性监测。
参考文献:
[1].Fraietta JA, Nobles CL, Sammons MA, et al. Disruption of TET2 promotes the therapeutic efficacy of CD19-targeted T cells. Nature. 2018;558(7709):307-312. doi:10.1038/s41586-018-0178-z
[2].Ruella M, Xu J, Barrett DM, et al. Induction of resistance to chimeric antigen receptor T cell therapy by transduction of a single leukemic B cell. Nat Med. 2018;24(10):1499-1503. doi:10.1038/s41591-018-0201-9
[3].Perica K, Jain N, Scordo M, et al. CD4+ T-Cell Lymphoma Harboring a Chimeric Antigen Receptor Integration in TP53. N Engl J Med. 2025;392(6):577-583. doi:10.1056/NEJMoa2411507
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:揭示小细胞肺癌劫持神经元突触从而加速生长背后的分子机制 (2025-09-12)
- Nat Commun:口腔微生物界的“超级英雄”!科学家揭示细胞外遗传元素Inocle的发现与意义 (2025-09-12)
- Trends Biotechnol.:武汉大学陈刚/余自力等团队提出FACTORY全自动 EV 分离平台,把 EV 分离从“小作坊”直接升级成“标准化工厂” (2025-09-12)
- EMBO Mol Med:罕见基因突变有望揭示肠道干细胞的再生奥秘 (2025-09-11)
- STTT:打断肿瘤的“狗腿”!科学家发现,抑制中性粒细胞的STAT3,会让中性粒细胞“改邪归正”,促进T细胞抗癌 (2025-09-11)
- Cell:IL-25诱导的记忆2型固有淋巴细胞,强化黏膜免疫 (2025-09-11)
- Nature Medicine:靶向休眠肿瘤细胞,预防乳腺癌复发 (2025-09-11)
- PLoS Biol:肠道真菌与人类健康——科学家揭秘基因与微生物的神秘联系! (2025-09-11)
- Nature重磅:“装甲型”CAR-T治疗实体瘤新突破,细胞因子精准“爆破”且全身毒性归零 (2025-09-11)
- 【9·10致敬全体教师】2025细胞外囊泡大会(厦门站)免费票速抢!! (2025-09-10)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















