2025年5月Cell期刊精华 |
 |
2025年5月份已经结束,5月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.
DOI: 10.1016/j.cell.2025.04.019
在信息飞速传播的当今世界,视觉作为人类获取信息的关键渠道,其重要性不言而喻。从情侣间的深情对视,传递着爱意与情绪,到我们日常观察世界、识别物体,视觉都发挥着核心作用。然而,人类的视觉存在局限,仅能感知 400 - 700 纳米的可见光,对于占太阳辐射能量半数以上的红外光却无能为力。这种感知局限,犹如让我们在探索世界的道路上戴上了 有色眼镜 ,错过了诸多精彩。
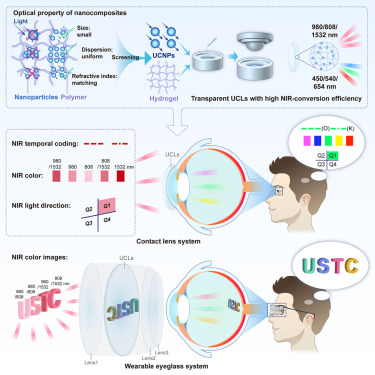
但一项前沿研究有望打破这一桎梏,它利用上转换隐形眼镜(UCLs),为人类开启近红外(NIR)视觉之门,赋予我们前所未有的视觉体验,极大地拓展信息获取维度,其意义堪比视觉领域的 哥白尼式革命 。
此项研究旨在突破人类视觉的物理局限,开发非侵入式、可穿戴的近红外视觉系统,使人类能够直接感知近红外光的时空与色彩信息。传统红外探测设备如夜视仪等,依赖外部能源、结构复杂且难以与人眼融合。而上转换隐形眼镜的问世,有望让人类无需借助复杂仪器,仅凭肉眼就能感知近红外光,这不仅在军事、救援等领域具有广泛应用前景,更在日常生活中为人类带来全新的视觉体验,拓宽我们对世界的认知边界。
2.
DOI: 10.1016/j.cell.2025.04.038
在一项新的研究中,杜克大学医学院开发的一种实验性药物可能提供强大的止痛效果,而不会产生阿片类药物的危险副作用。相关研究结果发表于《细胞》(Cell)杂志。
这种药物被称为SBI-810,属于新一代化合物,旨在靶向神经和脊髓上的受体。虽然阿片类药物会不加区别地淹没多个细胞通路,但SBI-810作为一种非阿片类治疗方法,采用了一种更的方法,仅激活一个特定的止痛通路,从而避免了与成瘾相关的欣快感。
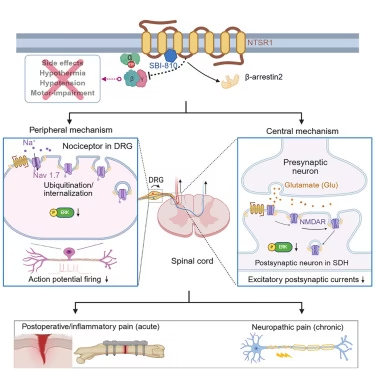
根据这项研究,在小鼠测试中,SBI-810单独使用时效果良好,并且当与阿片类药物联合使用时,能在更低剂量下提高阿片类药物的有效性。
SBI-810旨在靶向大脑中的神经紧张素受体1(neurotensin receptor 1)。通过使用一种称为偏向激动(biased agonism)的方法,它激活了一个与止痛相关的特定信号 -抑制蛋白2( -arrestin-2),同时避免了可能引起副作用或成瘾的其他信号。
3.
DOI: 10.1016/j.cell.2025.04.032
来自加州大学洛杉矶分校的一项新研究表明,一种广泛使用的抗抑郁药物可能有助于系统对抗癌症。它发现,选择性5-羟色胺再摄取抑制剂(SSRIs)显著增强了T细胞对抗癌症的能力,并在小鼠和人类肿瘤模型中抑制了多种类型肿瘤的生长。相关研究结果发表于《细胞》(Cell)杂志。
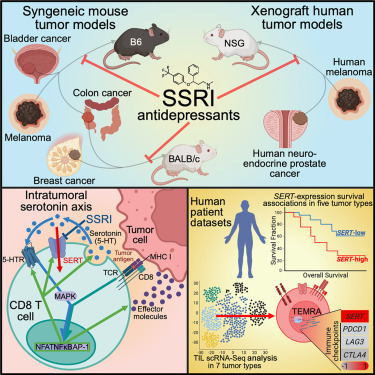
论文共同通讯作者、加州大学洛杉矶分校伊利和伊迪丝-博德再生医学与研究中心Lili Yang博士说, 事实证明,SSRIs不仅能让我们的大脑更快乐;它们还能让我们的T细胞更快乐 即使在它们对抗肿瘤的时候也是如此。几十年来,这些药物一直被广泛且安全地用于治疗,因此将其用于癌症治疗将比开发全新疗法容易得多。
该团队还研究了将SSRIs与现有癌症疗法相结合是否能改善治疗效果。他们在黑色素瘤和结肠癌小鼠模型中测试了SSRI和抗PD-1抗体(一种常见的免疫检查点阻断(ICB)疗法)的组合。ICB疗法通过阻断通常抑制免疫细胞活性的免疫检查点分子,使T细胞更有效地攻击肿瘤。
他们的实验结果令人震惊:在所有接受治疗的小鼠中,该组合显著缩小了肿瘤大小,甚至在某些情况下实现了完全缓解。Yang实验室研究生James Elsten-Brown说, 免疫检查点阻断疗法在少于25%的患者中有效。如果一种安全且广泛可用的药物,如SSRI,能够使这些疗法更有效,那将产生巨大的影响。
4.
DOI: 10.1016/j.cell.2025.04.041
在一项新的研究中,由来自路德维格癌症研究所的Asael Roichman和Joshua Rabinowitz领导的一个研究团队发现了饮食、肠道微生物与癌症治疗效果之间令人惊讶的联系。该研究有助于解释为何称为PI3激酶(PI3K)抑制剂的药物在实体瘤患者中未能实现一致且持久的癌症控制,其中这类药物会破坏促使异常增殖的一种异常激活的生化信号通路。相关研究结果发表在Cell杂志上。
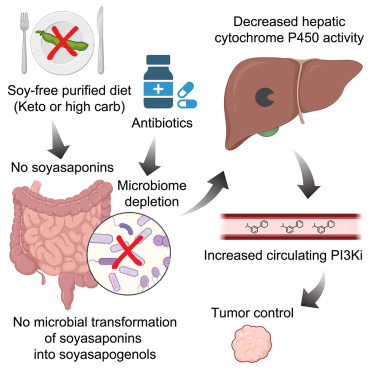
Rabinowitz说, 许多物并非对所有患者都同样有效,而出现这种差异的一种新可能是饮食在其中起到了作用。我们在这项研究中发现,饮食确实可以改变临床前模型中癌症治疗的效果,而且是以一种与其即时营养作用无关、出乎意料的方式。事实证明,植物性食物中的某些小分子会被小鼠体内的共生肠道细菌转化为化合物,这些化合物会激活肝脏,使其更快地清除PI3K抑制剂,从而降低药物的疗效。
Roichman补充道, 虽然我们在这项研究中关注的是PI3K抑制剂,但参与清除这些药物的肝脏酶也会分解许多其他药物。这表明我们的研究结果可能与用于治疗癌症和其他疾病的多种药物都相关。
5.
DOI: 10.1016/j.cell.2025.04.025
在一项具有开创性的研究中,来自英国弗朗西斯-克里克研究所(Francis Crick Institute)的研究人员成功构建了第一个成熟人类羊膜囊的三维模型。这种称为 原肠胚形成后类羊膜 (post-gastrulation amnioid, PGA)的新型干细胞模型,能够精确重现受精后两周至四周内的关键发育阶段,为理解人类早期发育提供了全新的视角,并为医学领域带来了新的希望。
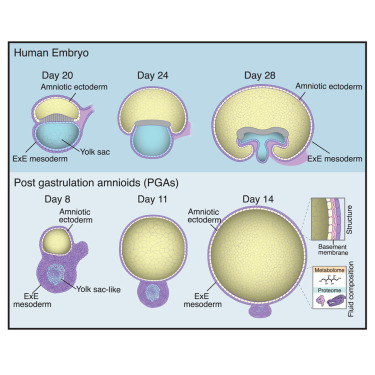
羊膜是哺乳动物胚胎中的一种重要组织,它形成一个充满羊水的囊,为胚胎提供保护和营养支持。然而,由于技术限制和伦理问题,科学家们一直难以深入研究羊膜的形成和功能。传统干细胞模型无法捕捉人类发育的后期阶段,而人类胚胎研究又受限于14天的研究期限。这使得羊膜的详细研究成为科学界的难题。
在这项研究中,研究人员通过一系列创新步骤,利用两种化学信号在48小时内诱导人类胚胎干细胞(hESCs)进行自我组装,成功构建了PGA模型。这些模型不仅在结构上与人类羊膜囊极为相似,还模拟了羊水的成分。研究显示,超过90%的PGA在第10天形成了囊状结构,并且能够在90天内持续扩大,无需额外信号输入。
6.
DOI: 10.1016/j.cell.2025.04.021
在当今社会,人类对甜食的钟爱已演变成一种普遍的 甜蜜负担 。据,美国人均每年摄入的甜食量已飙升至超过100磅,而在1800年,这一数字仅为18磅。
为了应对这一日益严峻的公共健康挑战,哥伦比亚大学的研究人员取得了突破性进展。他们首次成功绘制出人类甜味受体的三维结构图,这项发表在《Cell》杂志上的研究成果,有望引领我们迈向一个全新的时代,设计出能够有效调节人类对糖渴望的新型甜味受体调节剂。
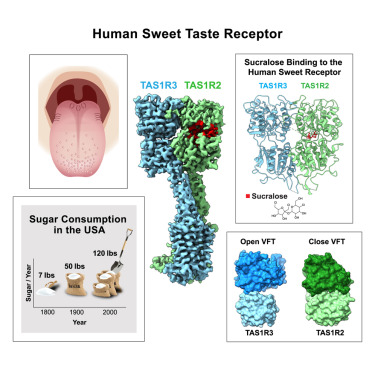
糖在肥胖症中扮演的角色不容忽视。目前,我们使用的人工甜味剂虽可替代糖,但无法有效改变我们对糖的强烈渴望。 论文共同第一作者、哥伦比亚大学祖克曼研究所Charles Zuker博士实验室博士后研究员Juen Zhang博士指出。我们的舌头上的甜味受体能够敏锐地检测到从普通砂糖(蔗糖)到鸡蛋中的抗菌酶等多种甜味化学物质。与其他苦味、酸味受体不同,甜味受体的进化目的并非追求高灵敏度,而是促使我们偏爱富含糖分的食物以获取能量,这也解释了为何我们需要大量甜食才能满足对甜味的向往。
研究人员通过创新的方法,历经约三年时间的努力,克服了这种蛋白在实验室细胞培养中的重重困难,最终成功绘制出人类甜味受体的结构图。论文共同第一作者、Zuker实验室博士生Zhengyuan Lu指出: 单是获得用于绘制结构图的纯化蛋白,就耗费了我们三年时间,尝试了150多种不同的制备方法。 随后,团队利用低温电镜(cryo-EM)技术对人类甜味受体进行了分析。该技术通过向冻结在溶液中的分子发射电子束,从不同角度捕捉分子的快照,从而在原子水平上重建其三维结构。
7.
DOI: 10.1016/j.cell.2025.04.022
在一项新的研究中,来自中国科学院生物物理研究所和北京理工大学的研究人员发现了细菌抵御病毒感染的一种关键机制。相关研究结果发表在Cell杂志上。
这项研究揭示了基于环状寡核苷酸的抗噬菌体信号系统(cyclic oligonucleotide-based anti-phage signaling system, CBASS)免疫机制激活过程中合成的环状二核苷酸(CDN)如何触发磷脂酶效应蛋白的丝状组装,其中磷脂酶效应蛋白通过破坏膜来执行下游免疫反应。
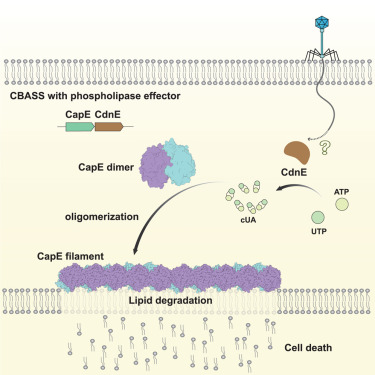
CBASS 是细菌中一种重要的先天性抗病毒防御机制,其核心效应模块在原核生物和真核生物免疫系统中都是进化保守的。虽然以前的研究发现 CDN是关键的信号传导分子,但它们如何激活下游效应分子的确切分子细节仍不清楚。
研究人员以 CBASS 系统中具有代表性的磷脂酶效应蛋白CapE 为研究对象,采用低温电子镜和 X 射线晶体学相结合的综合方法,确定了它在三种不同状态下的结构:非活性二聚体、与 CDN 结合的高阶组装体和与底物模拟结合的催化模拟体。这些结构快照共同捕捉到了 CapE 激活背后的全部构象转变。
8.
DOI: 10.1016/j.cell.2025.04.017
在一项发表在Cell杂志上的新研究中,来自巴塞罗那基因组调控中心的研究人员首次报道了生成式人工智能设计合成分子,从而成功控制健康哺乳动物细胞中的基因表达。
他们创造了一种人工智能工具,它能想象出自然界中从未见过的DNA调控序列。他们可以让该模型根据自定义标准创建合成的DNA片段,例如, 在干细胞中开启这个基因,使其变成红血细胞,而不是血小板 。
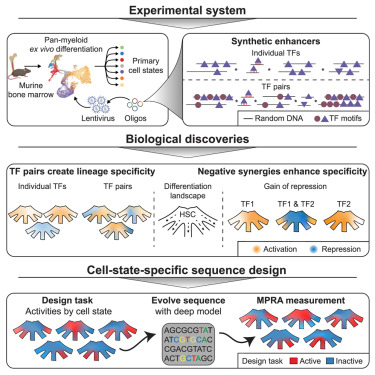
然后,这种模型会预测特定细胞类型所需的基因表达模式需要哪种 DNA碱基(A、T、C、G)组合。然后,他们就可以用化学方法合成大约 250 个碱基的 DNA 片段,并将其添加到病毒中,以便将后者递送到细胞中。
作为概念验证,研究人员要求人工智能设计合成片段,从而在某些细胞中激活编码荧光蛋白的基因,同时不改变基因表达模式。他们从头开始创建了这些片段,并将其放入小鼠血细胞中,在那里在随机位置与基因组融合。他们的实验结果与预测完全一致。
9.
DOI: 10.1016/j.cell.2025.03.041
在癌症免疫疗法领域,CAR-T细胞疗法无疑是颗璀璨明珠。它通过基因修饰患者T细胞,使其表达能特异识别癌细胞的嵌合抗原受体(CAR),从而精准摧毁癌细胞。这项技术已成功应用于多种血液癌症治疗,包括急性淋巴细胞、和特定类型,并在实体瘤临床试验中展现出巨大潜力。
然而,随着CAR-T细胞疗法广泛应用,一个令人担忧的问题逐渐浮现:患者接受治疗后常报告出现 脑雾 现象,表现为记忆力减退和注意力难以集中。近期,斯坦福大学医学院领导的一项新研究在《Cell》杂志上发表,揭示了CAR-T细胞疗法可能导致的认知障碍问题。
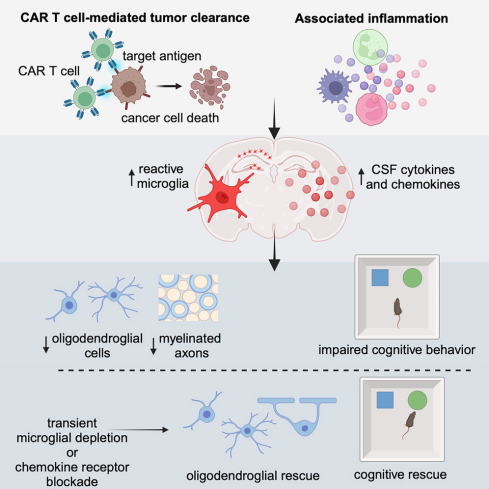
研究团队在小鼠模型上展开广泛实验,测试CAR-T细胞疗法对认知功能的影响。他们构建了多种小鼠模型,包括弥漫性脑桥胶质瘤(DIPG)、急性(ALL)和模型,以评估CAR-T细胞疗法对系统(CNS)和非CNS癌症的认知影响。通过新型物体识别测试(NORT)和自发交替T迷宫测试(T Maze),研究人员发现,无论癌症是否起源于大脑、扩散到大脑还是完全位于大脑外,接受CAR-T细胞疗法的小鼠均表现出轻度认知障碍,表现为对新物体的反应迟钝和在迷宫中导航能力下降。
研究进一步揭示了认知障碍的潜在机制。实验结果显示,CAR-T细胞疗法后,小胶质细胞(大脑中的免疫细胞)被激活,释放炎症分子(如细胞因子和趋化因子),这些分子对少突胶质细胞(负责生成髓鞘的脑细胞)具有毒性。髓鞘损伤导致神经信号传递效率下降,从而引发认知障碍。研究人员通过流式细胞术、免疫组织化学和电子显微镜技术,分析了小胶质细胞的活性、少突胶质细胞前体细胞(OPCs)和成熟少突胶质细胞的数量变化,以及髓鞘超微结构的改变。他们还检测了脑脊液(CSF)中细胞因子和趋化因子水平,以评估CAR-T细胞疗法后的神经炎症反应。
10.
DOI: 10.1016/j.cell.2025.04.015
现代的HIV医学基于一种常见的基因突变。丹麦人口中约有 18%-25% 的人携带这种称为CCR5delta32的基因突变,这种突变可使他们对 HIV 产生抵抗力甚至免疫力。这些知识被用于开发现代病毒治疗方法。在此之前,人们还不知道这种基因突变发生的时间、地点和原因。
如今,来自哥本哈根大学的研究人员在一项新的研究中通过使用先进的 DNA 技术解开了这个基因之谜。他们追溯到了这种基因突变产生的时间和地点,以及它如何保护我们的祖先免受古代疾病的侵袭。相关研究结果发表于2025年5月5日在线发表在Cell杂志上。
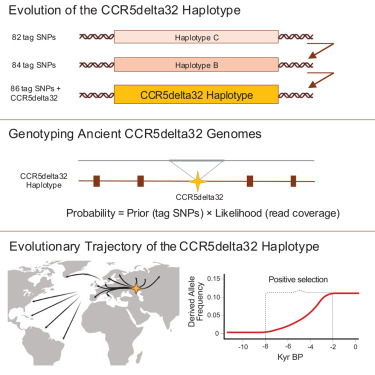
论文共同通讯作者、哥本哈根大学诺和诺德会基础代谢研究中心的Simon Rasmussen教授说, 事实证明,这种基因突变产生于6700年至9000年前生活在黑海附近地区的一个人身上。HIV是一种相对较新的疾病 不到 100 年的历史,因此,几千年前出现的一种基因突变也能抵御像HIV这样的现代病毒,这几乎是巧合,也非常令人着迷。
为了确定这种基因突变产生的时间和地点,研究人员首先通过分析全球 2000 名活人的遗传物质绘制了基因突变图谱。然后,他们开发了一种基于人工智能的新方法,从古老的骨骼中识别出古人DNA中的基因突变CCR5delta32。他们研究了从石器时代早期到维京时代的900多具骨骼的数据。
论文共同第一作者、哥本哈根大学诺和诺德基金会基础代谢研究中心高级研究员Kirstine Ravn说, 通过观察这个大型数据集,我们可以确定这种基因突变产生的时间和地点。在一段时期内,这种突变完全不存在,但后来突然出现,并以令人难以置信的速度迅速扩散。当我们把这一点与当时人类迁徙的知识结合起来时,我们就能确定这种基因突变产生的地区。
因此,研究人员能够在 9000 年前黑海地区的一个人身上找到这种基因突变,而所有这种基因突变的携带者都是这个人的后代。(100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nat Commun:人类肝癌治疗新曙光!科学家发现“阿喀琉斯之踵” (2025-05-31)
- Nature:揭示人类特有的DNA增强子与大脑发育和神经元增殖有关 (2025-05-30)
- Sci Adv:一种新的长链非编码RNA可能成为前列腺癌的治疗靶点 (2025-05-30)
- AACR2025:靶向 ICAM (2025-05-30)
- 2025年5月Cell期刊精华 (2025-05-30)
- Cell子刊:舒易来团队报道AAV基因治疗后,遗传性耳聋患者的听力恢复情况 (2025-05-30)
- Cell子刊:陈迪/黄慧琳/梁洪青团队揭示m6A修饰抑制体细胞向生殖细胞转化的机制 (2025-05-30)
- 英矽智能再发Nature子刊:利用生成式AI设计口服抗癌药,已获批临床试验 (2025-05-30)
- Cancer Res:靶向PRC2有望让CAR (2025-05-30)
- Science:新研究颠覆了人类对细胞如何分裂的传统观点!母细胞形状决定子细胞命运 (2025-05-30)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















