CD:一线治疗后进展的ER阳性晚期乳腺癌患者,PI3K抑制剂或许是治疗新选择 |
 |
来源:奇点糕 2022-12-02 11:56
这项研究发现了Alpelisib单药治疗在一线治疗后进展的ER+HER2-乳腺癌患者中展现出了良好的疗效,为内分泌治疗失败的患者提供了新的选择。磷脂酰肌醇3-激酶(PI3K)信号通路在调控细胞生长、代谢和存活方面发挥重要作用[1]。在各种肿瘤中,PI3K信号通路的失调非常常见,尤其是PIK3CA基因的突变[2,3]。
在中,约40%的雌激素受体阳性/人表皮生长因子受体2阴性(ER+HER2-)乳腺癌和20%的三阴性乳腺癌(TNBC)存在PI3K信号通路的改变[3-7]。
Alpelisib是一种PI3K 的选择性抑制剂,在PIK3CA突变的激素受体阳性/人表皮生长因子受体2阴性(HR+HER2-)的晚期乳腺癌患者中,Alpelisib联合氟维司群取得了显著疗效(SOLAR-1研究)[8]。
但截至目前,Alpelisib在乳腺癌后线治疗中的作用仍然未知。其次,Alpelisib能否在TNBC患者中发挥作用也是一个值得思考的问题。此外,还有研究显示,Alpelisib引起的高血糖和高胰岛素血症可能通过胰岛素/胰岛素样生长因子通路恢复PI3K的活性[9,10]。
针对以上问题,彼得 麦克卡勒姆癌症中心的Sherene Loi和Sarah-Jane Dawson研究团队,开展了一项单中心、开放标签、II期临床试验(NCT02506556),主要探究了Alpelisib单药在经治PIK3CA突变晚期乳腺癌中的疗效,相关结果近期发表在著名期刊Cancer Discovery上[11]。
总的来说,在一线治疗后进展的,存在PIK3CA突变的晚期ER+HER2-乳腺癌患者中,Alpelisib显示出不错的疗效(客观缓解率[ORR]为30%,临床受益率[CBR]为36%)。

论文首页截图
这项研究共纳入了43名一线治疗后进展的晚期乳腺癌患者,其中33名ER+HER2-乳腺癌患者,10名TNBC患者。所有患者中位年龄为60岁,且均已绝经(基线情况见下图)。

患者基线数据
研究的主要终点是根据实体瘤疗效评价标准1.1(RECIST1.1)评估的ORR。次要终点包括CBR以及无进展生存期(PFS)。

研究流程图
整体上看,有62.7%(n=27/43)的患者出现至少1次与Alpelisib相关的3级不良事件,28%(n=12/43)的患者出现与Alpelisib相关的严重不良事件。最常见的3/4级不良事件包括高血糖(32.6%,n=14/43),斑丘疹(25.6%,n=11/43),结肠炎(7.0%,n=3/43)和腹泻(7.0%,n=3/43)。
在疗效方面,数据截止时的中位随访时间为44.6个月。在意向ER+HER2-乳腺癌队列中,ORR为30%(n=10/33),CBR为36%(n=12/33),中位PFS为4.6个月(95%CI:3.7-7.3),中位总生存期(OS)为16.1个月(95%CI:8.5-34.5)。而在TNBC队列中ORR和CBR均为0%,由于缺乏有效性,该队列的招募被终止。
在Alpelisib引起的胰岛素抵抗方面,研究团队通过检测糖化血红蛋白(HbA1C)、C肽、空腹血糖水平和胰岛素抵抗的稳态模型(HOMA2-IR)对Alpelisib的代谢调控作用进行探究。结果显示,患者HbA1C、C肽、空腹血糖水平和HOMA2-IR均在治疗过程中显著升高。这提示Alpelisib治疗确实能引起高血糖和高胰岛素血症。
接下来,研究团队进一步探究了Alpelisib引起的高胰岛素血症,是否会恢复PI3K通路的活性。结果显示,与基线时相比,接受治疗后有响应的患者在第一次抽血检查时,C肽和HOMA2-IR的水平都发生了升高。但在整个治疗过程中C肽和HOMA2-IR的水平变化与患者响应程度无关。这提示目前尚没有证据表明治疗引起的高胰岛素血症可以引起治疗抵抗和肿瘤进展。
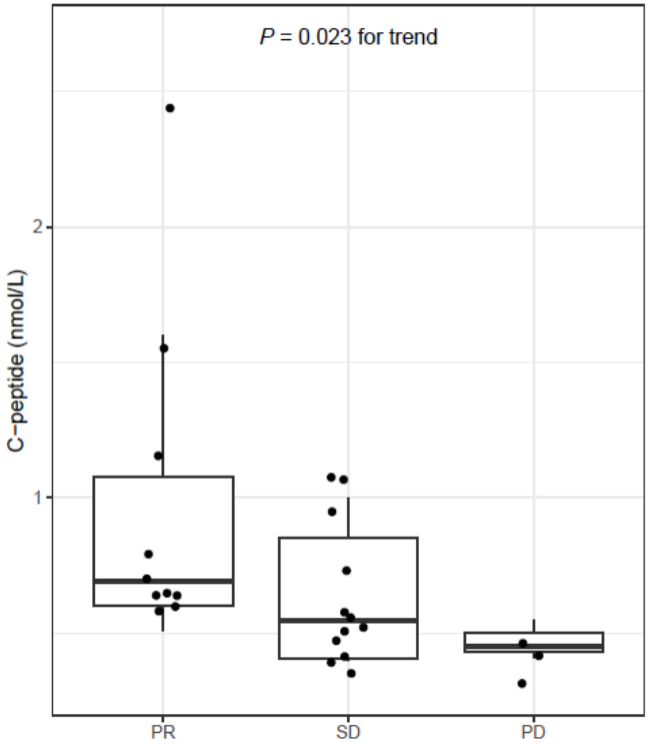
ER+HER2-乳腺癌队列中基线时C肽水平与患者响应的关系
研究团队探究了循环肿瘤DNA(ctDNA)突变水平与患者响应之间的关系。在ER+HER2-乳腺癌队列中,尽管基线时PIK3CA突变的ctDNA水平与患者ORR和CBR无关。但是,在Alpelisib治疗第8周时,与疾病稳定(SD)或疾病进展(PD)的患者相比,发生部分缓解(PR)的患者ctDNA水平的下降幅度更大。
此外,治疗期间,PIK3CA突变的ctDNA水平从基线至第8周的下降与CBR和PFS改善显著相关(HR=0.24,95%CI:0.083-0.67,P=0.0065)。
这些结果提示治疗过程中PIK3CA突变的ctDNA水平变化可以用来监测患者对Alpelisib的响应情况。
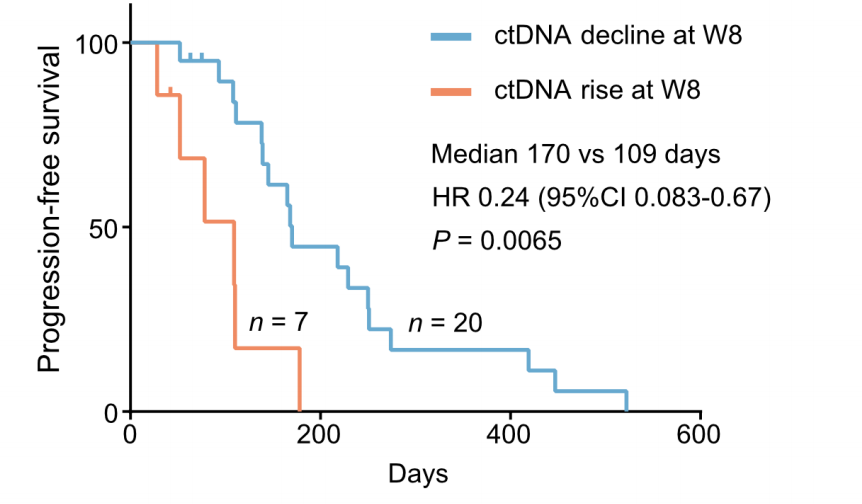
ER+HER2-乳腺癌队列中患者PIK3CA突变的ctDNA水平与患者响应的关系
ER+HER2-乳腺癌患者对于内分泌治疗产生耐药的一个关键机制是雌激素受体1(ESR1)突变[12]。因此研究人员进一步探究了ctDNA中的ESR1突变,与ER+HER2-乳腺癌患者对Alpelisib响应的关系。
结果发现,基线时检测血浆ESR1突变也与CBR和PFS改善显著相关(HR=0.22,95%CI:0.078-0.60,P=0.003),这提示可以通过检测基线时ctDNA中ESR1突变,预测患者对Alpelisib单药治疗的响应情况。
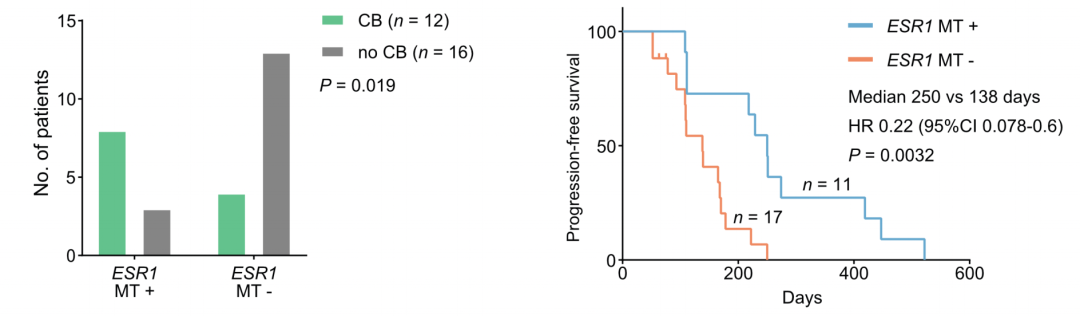
ER+HER2-乳腺癌队列中基线时患者ctDNA中ESR1突变与患者响应的关系
总的来讲,这项研究发现了Alpelisib单药治疗在一线治疗后进展的ER+HER2-乳腺癌患者中展现出了良好的疗效,为内分泌治疗失败的患者提供了新的选择。
参考文献:
[1] Fruman DA, Chiu H, Hopkins BD, Bagrodia S, Cantley LC, Abraham RT. The PI3K Pathway in Human Disease.Cell. 2017;170(4):605-635. doi:10.1016/j.cell.2017.07.029
[2] Zehir A, Benayed R, Shah RH, et al. Mutational landscape of metastatic cancer revealed from prospective clinical sequencing of 10,000 patients [published correction appears in Nat Med. 2017 Aug 4;23 (8):1004].Nat Med. 2017;23(6):703-713. doi:10.1038/nm.4333
[3] Bailey MH, Tokheim C, Porta-Pardo E, et al. Comprehensive Characterization of Cancer Driver Genes and Mutations [published correction appears in Cell. 2018 Aug 9;174(4):1034-1035].Cell. 2018;173(2):371-385.e18. doi:10.1016/j.cell.2018.02.060
[4] Cancer Genome Atlas Network. Comprehensive molecular portraits of human breast tumours.Nature. 2012;490(7418):61-70. doi:10.1038/nature11412
[5] Pereira B, Chin SF, Rueda OM, et al. The somatic mutation profiles of 2,433 breast cancers refines their genomic and transcriptomic landscapes.Nat Commun. 2016;7:11479. Published 2016 May 10. doi:10.1038/ncomms11479
[6] Berger AC, Korkut A, Kanchi RS, et al. A Comprehensive Pan-Cancer Molecular Study of Gynecologic and Breast Cancers.Cancer Cell. 2018;33(4):690-705.e9. doi:10.1016/j.ccell.2018.03.014
[7] Razavi P, Chang MT, Xu G, et al. The Genomic Landscape of Endocrine-Resistant Advanced Breast Cancers.Cancer Cell. 2018;34(3):427-438.e6. doi:10.1016/j.ccell.2018.08.008
[8] Andr F, Ciruelos E, Rubovszky G, et al. Alpelisib forPIK3CA-Mutated, Hormone Receptor-Positive Advanced Breast Cancer.N Engl J Med. 2019;380(20):1929-1940. doi:10.1056/NEJMoa1813904
[9] Fox EM, Kuba MG, Miller TW, Davies BR, Arteaga CL. Autocrine IGF-I/insulin receptor axis compensates for inhibition of AKT in ER-positive breast cancer cells with resistance to estrogen deprivation.Breast Cancer Res. 2013;15(4):R55. doi:10.1186/bcr3449
[10] Hopkins BD, Pauli C, Du X, et al. Suppression of insulin feedback enhances the efficacy of PI3K inhibitors [published correction appears in Nature. 2018 Aug 29;:].Nature. 2018;560(7719):499-503. doi:10.1038/s41586-018-0343-4
[11] Savas P, Lo LL, Luen SJ, et al. Alpelisib Monotherapy for PI3K-Altered, Pretreated Advanced Breast Cancer: A Phase II Study.Cancer Discov. 2022;12(9):2058-2073. doi:10.1158/2159-8290.CD-21-1696
[12] Hermida-Prado F, Jeselsohn R. TheESR1Mutations: From Bedside to Bench to Bedside.Cancer Res. 2021;81(3):537-538. doi:10.1158/0008-5472.CAN-20-4037
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 《自然· 医学》:按照膳食指南吃可能还不够!最新临床试验显示,即使遵照指南要求吃饭,多吃超加工食品仍会阻碍减重 (2025-08-06)
- 施一公团队发表最新PNAS论文 (2025-08-06)
- 致癌代谢物2HG竟是肥胖“隐形推手”?!Nat Metabol 最新研究中科学家揭秘肥胖发生新机制 (2025-08-05)
- Sci Adv:科学家有望重新训练中性粒细胞来靶向治疗乳腺癌 (2025-08-05)
- 特洛伊木马:复旦大学最新论文登上Cell子刊封面 (2025-08-05)
- TN:南京医科大学团队发现,长期运动可通过改善脑膜淋巴管结构和引流功能,减轻AD病理,并改善小鼠认知功能 (2025-08-05)
- 柳叶刀:塑料危机——对人类从摇篮到坟墓的健康威胁 (2025-08-05)
- Nature子刊:中山大学林浩添/陈崴团队开发AI模型,利用视网膜图像无创诊断慢性肾病 (2025-08-05)
- 四部分脱手!医疗科普不是“流量生意” (2025-08-05)
- 3000余人追踪35年!JAMA子刊:心血管病发前12年身体活动已下滑,发病后运动量暴跌78% (2025-08-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















