ACS Nano:张志文/李亚平/张翱合作开发智能仿生递药系统,改善肿瘤免疫治疗 |
 |
来源:生物世界 2022-12-21 11:06
该研究设计合成了酸敏感两亲性聚合物(PEG-PDPA)以及酶敏感吉西他滨前药(C14-Gem)并制备成胶束;通过巨噬细胞膜的覆盖制备成MNGs。检查点阻断是肿瘤治疗领域的革命性进展,但耐药导致仅有一小部分癌症患者对该疗法有响应。在某些肿瘤中,癌细胞可阻止淋巴细胞的浸润,且大部分浸润性淋巴细胞功能为耗竭状态。因此,如何促进淋巴细胞的浸润以及扭转淋巴细胞杀伤功能成为检查点阻断治疗的关键问题。
复旦大学药学院张志文团队、中国科学院上海药物研究所李亚平团队、上海交通大学药学院张翱团队合作,在ACS Nano期刊发表了题为:Macrophage Membrane-Coated Nano-Gemcitabine Promotes Lymphocyte Infiltration and Synergizes AntiPD-L1 to Restore the Tumoricidal Function的研究论文。
该并构建了一种负载吉西他滨前药的智能仿生递药系统(MNGs),用于提高瘤内淋巴细胞的浸润并进一步提高免疫检查点阻断剂的抗肿瘤效果。

该研究设计合成了酸敏感两亲性聚合物(PEG-PDPA)以及酶敏感吉西他滨前药(C14-Gem)并制备成胶束;通过巨噬细胞膜的覆盖制备成MNGs。由于巨噬细胞膜的仿生特性,MNGs能够在肿瘤部位蓄积并渗透进入肿瘤深部,提高肿瘤内部淋巴细胞的浸润以及免疫检查点PD-L1表达,协同PD-L1单抗重新激活淋巴细胞的抗肿瘤杀伤功能。
研究结果表明,与MNGs单药治疗组相比,MNGs+PD-L1单抗联合治疗组可使耗竭状态的CD3+CD8+T细胞和自然杀伤细胞分别减少31.77%和30.63%,而干扰素- 阳性亚型分别增加2.83倍和3.17倍。在多种肿瘤模型中产生可观的治疗效果。因此,MNGs为促进淋巴细胞的浸润和协同PD-L1单抗恢复淋巴细胞肿瘤杀伤能力提供了一种新思路。
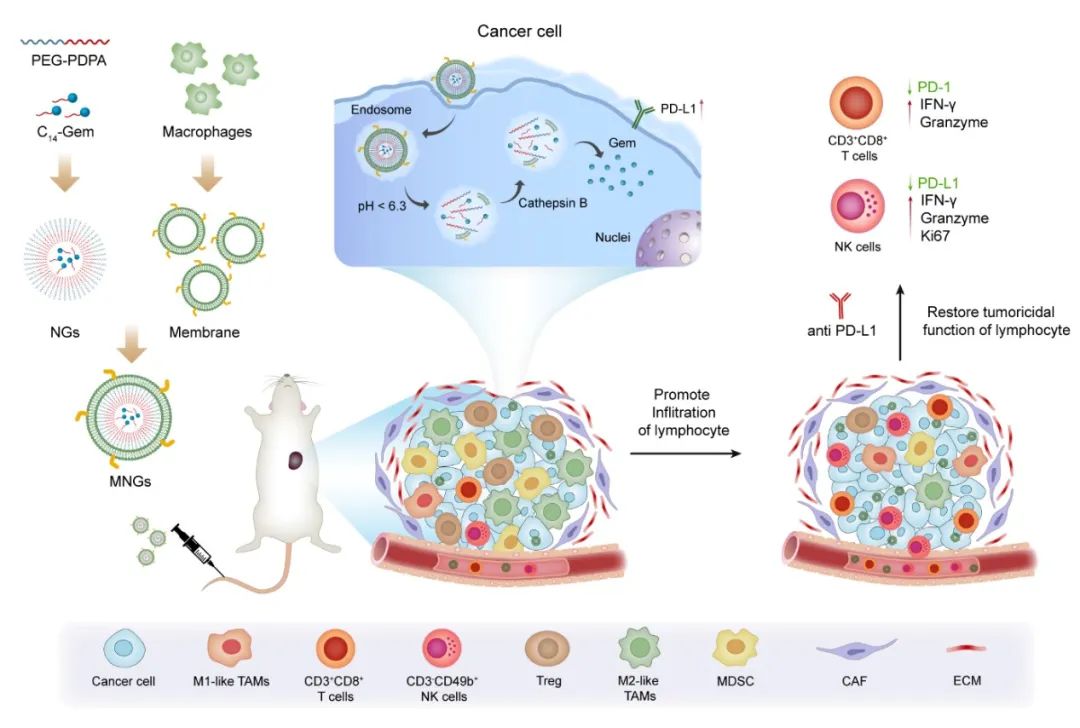 MNGs的制备及协同PD-L1抗体提高抗肿瘤免疫治疗效果
MNGs的制备及协同PD-L1抗体提高抗肿瘤免疫治疗效果
复旦大学张志文研究员、上海药物所李亚平研究员及上海交通大学张翱教授为论文共同通讯作者,上海药物所博士后李杰、上海药物所-复旦大学联合培养研究生吴瑶为论文第一作者。该论文得到国家重点研发计划、国家等项目资助。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 《自然· 医学》:按照膳食指南吃可能还不够!最新临床试验显示,即使遵照指南要求吃饭,多吃超加工食品仍会阻碍减重 (2025-08-06)
- 施一公团队发表最新PNAS论文 (2025-08-06)
- 致癌代谢物2HG竟是肥胖“隐形推手”?!Nat Metabol 最新研究中科学家揭秘肥胖发生新机制 (2025-08-05)
- Sci Adv:科学家有望重新训练中性粒细胞来靶向治疗乳腺癌 (2025-08-05)
- 特洛伊木马:复旦大学最新论文登上Cell子刊封面 (2025-08-05)
- TN:南京医科大学团队发现,长期运动可通过改善脑膜淋巴管结构和引流功能,减轻AD病理,并改善小鼠认知功能 (2025-08-05)
- 柳叶刀:塑料危机——对人类从摇篮到坟墓的健康威胁 (2025-08-05)
- Nature子刊:中山大学林浩添/陈崴团队开发AI模型,利用视网膜图像无创诊断慢性肾病 (2025-08-05)
- 四部分脱手!医疗科普不是“流量生意” (2025-08-05)
- 3000余人追踪35年!JAMA子刊:心血管病发前12年身体活动已下滑,发病后运动量暴跌78% (2025-08-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















