Science:改写教科书!细菌能够在基因组外从头生成新基因,以对抗病毒感染 |
 |
来源:生物世界 2024-08-19 09:08
这项颠覆性研究表明,DRT2系统执行了一种前所未有的免疫防御机制,该机制涉及通过非编码RNA(ncRNA)的滚环逆转录来指导DNA的从头合成,并通过程序化模板跳跃产生串联的cDNA重复序列。早在1958年,DNA双螺旋的发现者之一 弗朗西斯 克里克(Francis Crick)提出了著名的 中心法则 ,为遗传信息的传递构建一个大框架:DNA RNA 蛋白质。根据这一法则,DNA作为基因模板,转录生成RNA,RNA再翻译为蛋白质。
1970年,科学家们在一些病毒中发现了逆转录酶,这种酶可以将RNA逆转录成DNA,这为中心法则做出了重要补充,揭示了遗传信息并不只是单向流动,也可以实现从RNA DNA的逆向流动。
自遗传密码被破译以来,我们打开了生命的天书,通过阅读和解码我们的染色体,我们得以识别基因组中的基因,这种线性的生命法则被认为支配着所有的生命形式 从细菌到人类。
而哥伦比亚大学的研究人员的一项新研究表明,细菌打破了这一规则,它们可以创造出在细胞质中自由漂浮和短暂的基因,这一发现颠覆了染色体拥有细胞用来产生蛋白质的一整套完整遗传指令的观点,揭示了 隐藏基因 的存在。
具体来说,一种存在于细菌中的逆转录酶将非编码RNA作为模板来读取,从头生成新基因。然后,这一基因重新转录成RNA,当细菌被病毒感染时,RNA被翻译成保护性蛋白。相比之下,病毒的逆转录酶并不会产生新基因,它们只是简单地将将RNA逆转录为DNA。
这项研究强调了细菌逆转录酶以RNA为模板创造新基因的基因组编码潜力,是对中心法则这一遗传信息传递方式的挑战,也将改变我们看待基因组DNA线性编码遗传信息的传统范式。
该论文于2024年8月8日发表于Science期刊,并于5月8日在预印本平台bioRxiv上线,论文题为:De novo gene synthesis by an antiviral reverse transcriptase。

细菌通过部署多种防御系统来抵御病毒和其他入侵者,比如强大的免疫防御系统CRISPR,可以感知并靶向切割外来核酸,这也被改造为现在广泛应用的CRISPR基因编辑工具。
此外,细菌中还有一个更神秘的防御系统 防御相关逆转录酶(Defense-associated reverse transcriptas,DRT),该系统包含一种逆转录酶和一小段没有任何明确功能的神秘RNA。这个RNA序列似乎没有编码任何蛋白质,但其DNA产物的身份和功能在很大程度上仍然未知。
为了弄清楚这个系统是如何工作的,哥伦比亚大学的Samuel Sternberg和Stephen Tang领导的研究团队探索了肺炎克雷伯菌(Klebsiella pneumoniae)的防御相关逆转录酶产生的DNA分子。他们发现了一段非常长的DNA序列,它由许多相同的重复片段组成,并且每个片段都与一段神秘的RNA相匹配。
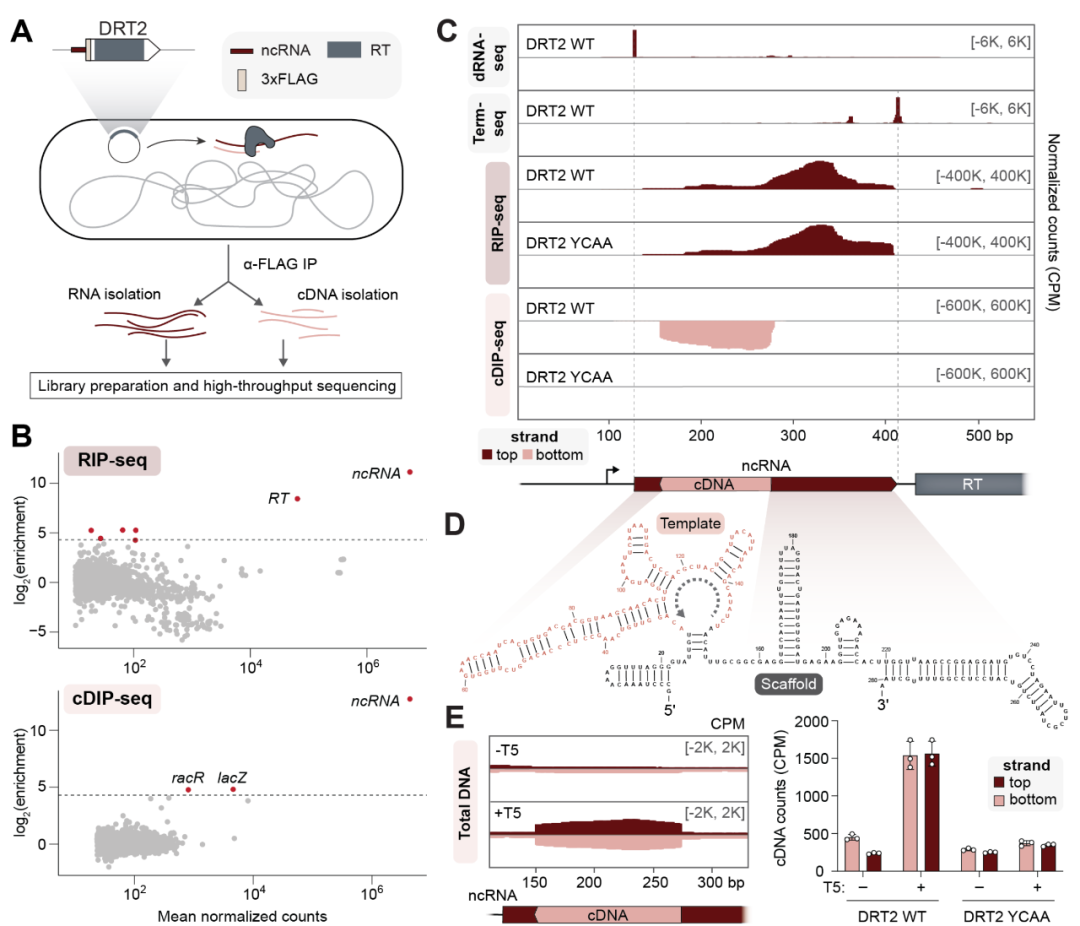
在体内系统发现DRT2逆转录底物和产物
众所周知,RNA可以形成复杂的高级结构,例如较长的RNA链可以形成发夹结构,从而使得原本距离较远的部分可以彼此靠近。研究团队发现,肺炎克雷伯菌的逆转录酶在RNA序列周围重复 绕圈 ,长RNA也像鞋带一样形成发夹结构,逆转录酶多次将相同的RNA分子写进DNA中,由此创造了一个重复的DNA序列。
这些重复的序列形成了一个可以编码蛋白质的开放阅读框(ORF)序列。研究团队将这个序列命名为Neo,意思是 永无止境的开放阅读框 (Never-Ending Open reading frame),致敬著名电影《黑客帝国》中的男主角救世主尼奥(Neo)。Neo缺少一个标志蛋白质末端序列,因此理论上可以无限制地翻译下去。
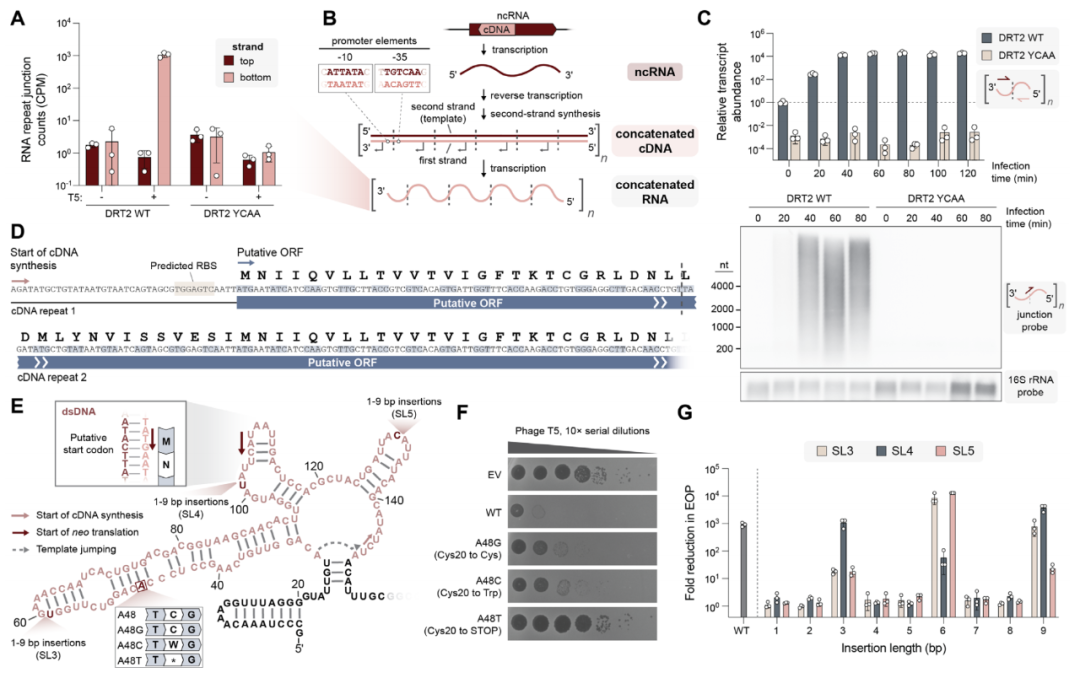
连接的cDNA产物包含一个永无止境的ORF Neo
接下来,研究团队发现肺炎克雷伯菌在被病毒(噬菌体)感染后会触发Neo蛋白的产生,并导致自身停止分裂。目前还不清楚Neo如何阻止被病毒感染的细菌的生长,AlphaFold预测的长链状态下的Neo形成了一系列螺旋,实验表明分解这些形状会阻碍Neo的毒性作用。
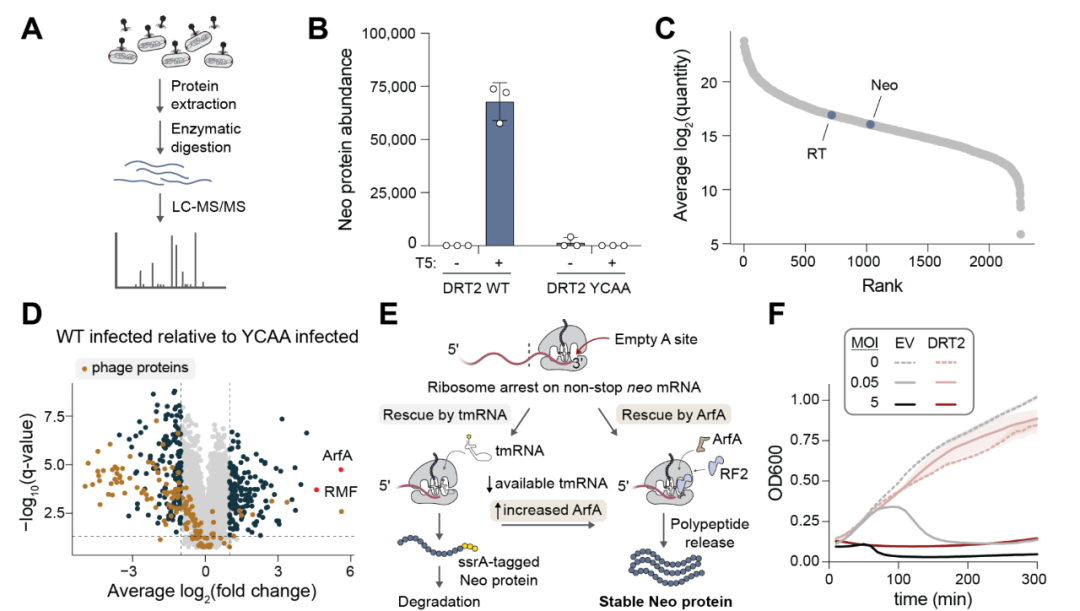
Neo蛋白诱导程序性细胞休眠
总的来说,这项颠覆性研究表明,DRT2系统执行了一种前所未有的免疫防御机制,该机制涉及通过非编码RNA(ncRNA)的滚环逆转录来指导DNA的从头合成,并通过程序化模板跳跃产生串联的cDNA重复序列。噬菌体感染触发第二链cDNA合成,导致长双链DNA(dsDNA)的产生。
值得注意的是,这种DNA产物可以有效转录,产生mRNA编码无终止密码子的、永无止境的ORF Neo,其翻译导致有效的细菌生长停滞,从而阻止病毒的复制、增殖和传播。

研究模式图
此外,系统发育分析和多种DRT2同源物的筛选进一步揭示了滚环逆转录和Neo蛋白功能的广泛保守性。这项工作强调了细菌逆转录酶以RNA为模板创造新基因的基因组编码潜力,对中心法则这一遗传信息传递方式发起挑战,并将改变我们看待基因组的方式。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 两篇《自然》:肺癌私联神经元!科学家首次发现小细胞肺癌细胞会在脑内与神经元形成突触,借助电信号促进肿瘤生长 (2025-09-16)
- Sci Adv:新型双特异性抗体有望成为抗击巨细胞病毒的“免疫特种兵” (2025-09-16)
- 《神经病学》:代糖或伤认知!8年随访发现,摄入较多代糖与记忆力、语言流畅性和整体认知能力下降速度提升32%、173%和62%相关 (2025-09-16)
- Nature子刊:超越ADC,中国博后发明ABC药物,重拳出击,精准靶向 (2025-09-16)
- Cell子刊:“滴血验癌”新突破,王延博/张硕等利用细胞外囊泡,精准检测10多种癌症 (2025-09-16)
- 47亿!派林生物易主中国生物,血液制品行业格局将重塑 (2025-09-15)
- 【9月16日直播预告】从样本到洞察:蛋白质组学智能实验室的自动化流程与AI高效赋能 (2025-09-15)
- 聚焦靶向蛋白降解、小核酸、多肽、细胞治疗等热点议题,与60+行业领袖共探生物医药未来。10月16-17日,深圳,期待您的加入! (2025-09-15)
- Nature子刊:个性化定制碱基编辑器,治疗致命血管疾病 (2025-09-15)
- 智力出现障碍的罪魁祸首!Cell Rep:两种“染色质管家”联手失控,神经元“身份混乱”致认知受损 (2025-09-15)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















