Nature:细菌须要共同的基因暗码才干在人肠道中生活 |
 |
2019年11月15日讯/BIOON/---人类的肠道是一个风险的处所。生涯在人肠道中的细菌会排出毒从来阻拦微者。不外,在一项新的研讨中,来自美国华盛顿年夜学的研讨人员报道每团体的肠道都带有本人的一套毒素---个别化的“暗码(passcode)”,必需处理这些毒素才干生活上去。相干研讨成果近期揭橥在Nature期刊上,论文题目为“Human gut bacteria contain acquired interbacterial defence systems”。
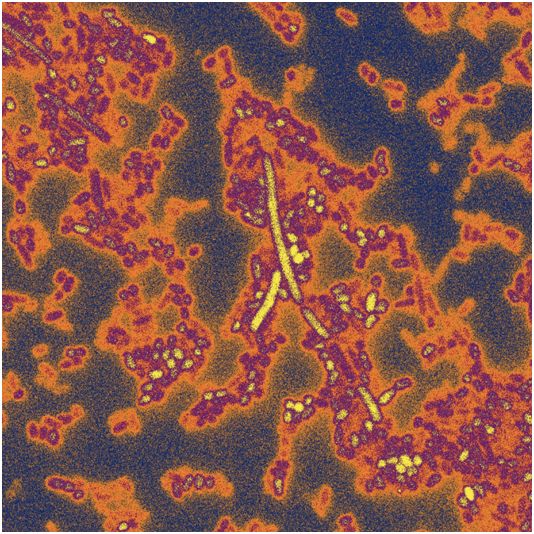 很多拟杆菌品种(在这张黑色显微照片中显示的是五种拟杆菌品种的混杂)存在于人类肠道中,并排泄毒素,细菌必需中和这些毒素才干生活,图片来自Kevin Cutler/Mougous Lab/UW/HHMI。
论文配合通信作者、华盛顿年夜学霍华德休斯医学研讨所研讨员Joseph Mougous说,这些研讨成果标明益生菌或活生物疗法(live biotherapeutics),即增进安康发展的微生物弥补剂,并没有一种放之四海而皆准的办法。他的团队的研讨任务是朝着弄清晰迷信家们若何能够为分歧的人定制无益微生物而迈出的较早的一步。
很多拟杆菌品种(在这张黑色显微照片中显示的是五种拟杆菌品种的混杂)存在于人类肠道中,并排泄毒素,细菌必需中和这些毒素才干生活,图片来自Kevin Cutler/Mougous Lab/UW/HHMI。
论文配合通信作者、华盛顿年夜学霍华德休斯医学研讨所研讨员Joseph Mougous说,这些研讨成果标明益生菌或活生物疗法(live biotherapeutics),即增进安康发展的微生物弥补剂,并没有一种放之四海而皆准的办法。他的团队的研讨任务是朝着弄清晰迷信家们若何能够为分歧的人定制无益微生物而迈出的较早的一步。
他说:“把持肠道微生物来增进安康有好多愿望,但尚不清晰在肠道中定植的规矩。”现在,迷信家们对若何假寓有了更好的懂得。
人类的肠道充斥细菌。粪便每克含有约1000亿个细菌细胞,肠道细菌的数目是人类细胞的10倍。Mougous说,这些微生物(统称为肠道微生物组)承当着各类各样的保护任务。他们消化食物,坚持肠道外表完好,供给维生素,并肃清无害。他说:“肠道微生物组对人类安康十分主要,这一点我们是晓得的。”
在过来的十年中,Mougous团队找出了一种称为VI型排泄零碎(VI secretion system)的进攻机制的细节。这种排泄零碎就像一个分子打针器,将毒素注入临近的细胞。这些毒素会毁坏细胞壁,扯破细胞膜并吞噬细胞的能量起源。他说:“它们长短常阴险的。”
应用免疫基因来中和这些毒素并维护本人。缺少准确基因的入侵者会从肠道中被踢出。 Mougous团队曾以为毒素和免疫基因像锁和钥匙一样成对呈现。然则对来自1000多团体类粪便样本的数据停止的剖析显示出令人受惊的器械。
作为一种肠道细菌,软弱拟杆菌(Bacteroides fragilis)的免疫基因远远超越了毒素基因。Mougous团队发明,一切这些额定的免疫基因实践上都属于其他细菌。这些细菌窃取了软弱拟杆菌的基因,从而维护它们本人免受软弱拟杆菌发生的毒素的损害。Mougous说,这意味着这些基因关于在肠道中生活至关主要。这是迷信家们以前所不晓得的。
包含微生物学家Benjamin Ross 在内的Mougous团队与华盛顿年夜学的Elhanan Borenstein(另一名论文配合通信作者)协作停止了基因组剖析。尔后,Borenstein搬到了以色列特拉维夫年夜学,Ross现在就职于美国达特茅斯学院。Mougous说:“这种协作十分风趣,这是由于它使我们两个团队都进入了新范畴。”
试验室中的试验标明这些免疫基因集合在可以在细菌菌株之间腾跃的DNA片断上。在试验室培育皿和活体小鼠中,付与这些基因的立刻对软弱拟杆菌的毒素发生抵御力。
更主要的是,这些研讨人员发明,人类粪便样品具有毒素和免疫基因的共同组合。 Mougous说:“是以,在一团体的微生物组中生活所须要的器械能够与另一团体的微生物组中有所分歧。”
他说,这些研讨成果可以说明为什么人们很难修补他们的微生物组构成。“将某些在肠道内定植的通用办法能够永远不会胜利,并且能够须要个别化。”(100医药网 100yiyao.com)
参考材料:
1.Benjamin D. Ross et al. . Nature, 2019, doi:10.1038/s41586-019-1708-z.
2.To survive in the human gut, bacteria need genetic "passcode"
https://phys.org/news/2019-10-survive-human-gut-bacteria-genetic.html
医药网新闻
- 相关报道
-
- Environ Sci Technol:污水处理厂排出的“隐形杀手”——纤维与碎片微塑料成抗生素耐药基因载体,加剧水环境健康风险 (2025-07-10)
- 不抽烟,为什么会得肺癌?Nature:科学家揭秘空气污染如何促进非吸烟人群肺癌的发生 (2025-07-10)
- 江南大学发表最新Cell子刊论文 (2025-07-10)
- 赛多利斯推出 iQue® 5 高通量流式细胞分析仪:快速、灵活、智能,重构高通量筛选体验 (2025-07-09)
- STTT:上中医/北中医团队最新成果证实,天然产物乙酰缬草三酯通过双重铁死亡机制,抑制肠癌的生长、转移和耐药 (2025-07-09)
- Nature系列综述:CAR-T在自身免疫疾病中异军突起,将面临哪些挑战? (2025-07-09)
- Cell Rep Med:癌症诊断新突破!细胞外囊泡“巨无霸”成为液体活检的黄金标记物 (2025-07-09)
- Fertil Steril:定制完美宝宝?基因编辑前夜的抉择——一文读懂PGT-M技术的是与非 (2025-07-09)
- Nat Cancer:科学家破解乳腺癌耐药新机制——γδ T细胞与巨噬细胞的“共谋” (2025-07-09)
- 无需植入支架!血管闭塞患者有了新选择 (2025-07-09)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















