光盘:代谢酶搞副业 癌王欣喜若狂! |
 |
来源:奇点蛋糕2022-11-14 09:34
该团队的研究工作揭示了代谢酶GOT2的非经典和非代谢功能,证明了GOT2也可以通过与核脂肪酸配体结合来调节PPAR转录活性,从而干扰免疫相关基因的表达,影响肿瘤生长的免疫环境。
癌症(PDAC)因其极高的死亡率而令人恐惧。虽然目前关于PDAC的几项监管研究已经获得了良好的临床效益,但考虑到PDAC的肿瘤微环境非常复杂,还需要许多研究挖掘来提供线索,以便继续提高免疫治疗的疗效。
代谢异常是肿瘤的重要特征之一。许多代谢酶在肿瘤细胞中异常表达。一方面,他们兢兢业业地做好本职工作,以满足肿瘤快速增殖的需要;另一方面,一些代谢酶还执行非经典的非代谢功能,参与基因表达的调节,并对细胞增殖、存活、凋亡和肿瘤微环境的重塑等生物活动产生影响[1]。
最近,俄勒冈健康与科学大学的Mara H. Sherman团队在《癌症发现》上发表了一篇重要的研究论文[2]。研究人员发现,PDAC细胞中一种看似不起眼的线粒体转氨酶GOT2具有重要的非经典和非代谢功能:它可以调节核脂肪酸的代谢,增强核转录受体PPAR的活性,促进COX2和其他免疫功能相关基因的上调,创造有利于PDAC生长的免疫环境。

报纸首页截图
顾名思义,大家都很熟悉的GOT2是一种位于线粒体内的代谢酶,可以将草酰乙酸转化为天冬氨酸,并通过NADPH维持细胞内的氧化还原平衡[3]。然而,也有一些证据表明,GOT2可以影响细胞之间的脂质代谢[4]。
考虑到脂质代谢在实体肿瘤进展中的关键作用,以及在PDAC检测到GOT2表达的异常上调[5,6],研究人员希望找出GOT2在PDAC进展中的作用,以及它作为线粒体代谢酶如何影响脂质代谢。
首先,研究人员分别构建了GOT2敲除和敲除PDAC细胞系。
体外研究发现,GOT2敲除或敲除对PDAC肿瘤细胞的增殖没有明显影响。然而,将PDAC细胞注射到免疫健康小鼠体内形成肿瘤后,发现与对照组相比,GOT2敲除组和敲除组的肿瘤生长进度明显减慢。然而,用增殖标记物KI-67染色的结果也显示肿瘤细胞的增殖能力没有改变,提示GOT2可能通过改变肿瘤生长环境来影响PDAC的进展。
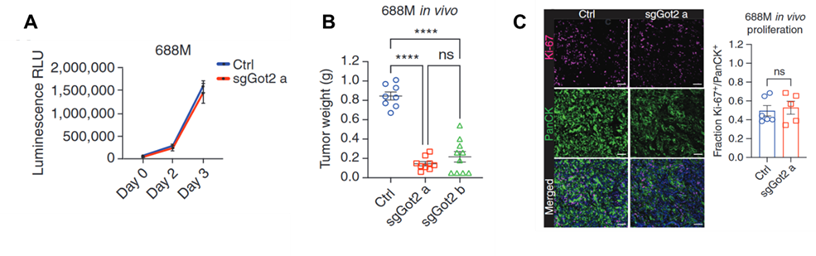
GOT2基因敲除对PDAC细胞的增殖没有影响。
接下来,研究人员丰富了与GOT2表达相关的信号通路,发现与免疫细胞分化、激活和粘附相关的通路与GOT2表达呈负相关。
此外,研究人员发现,在GOT2敲除组中有更多的CD4和CD8 T细胞浸润到肿瘤中,其中包括KI67和GranzymeB T细胞,它们起到了抗癌作用,AGR免疫抑制巨噬细胞的浸润比例也明显下降。
等等,难道仅仅是因为对照组和GOT2敲除组肿瘤大小的差异,才造成这些浸润免疫细胞的差异吗?
因此,在肿瘤发展的早期,研究人员利用小鼠之间肿瘤体积的微小差异,设置了几个时间点来检测肿瘤中的T细胞浸润率。发现GOT2基因敲除组肿瘤中T细胞的浸润率仍明显高于对照组。而且,当研究人员消除这些浸润性T细胞后,GOT2敲除组的肿瘤生长抑制作用就会消失。
这些结果表明,GOT2可能通过重塑肿瘤中的免疫环境来影响肿瘤的生长。
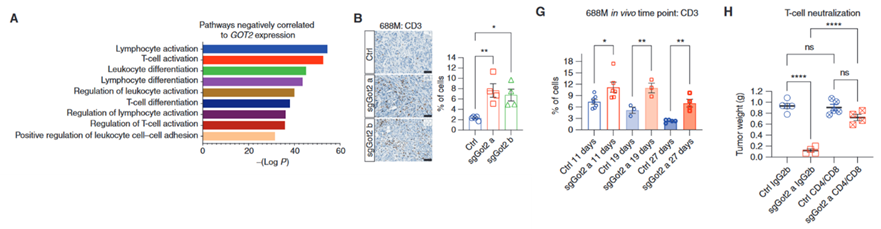
GOT2敲除增加T细胞浸润
位于PDAC肿瘤细胞线粒体上的GOT2如何影响周围的T细胞?
在仔细分析人类和小鼠PDAC组织后,研究人员发现一些GOT2位于肿瘤细胞的细胞核中。让人想起以前的发现
结果表明,在PDAC肿瘤细胞中,GOT2的表达与PPAR下游靶基因呈显著正相关。此外,发现敲除GOT2后,PDAC细胞核中的PPAR转录活性和PPAR下游靶基因的表达显著下调,包括编码COX2的基因PTGS2。
研究表明,肿瘤细胞中的COX2可以促进微环境中的T细胞耗竭,因此研究人员锁定了这一研究方向。
>他们在GOT2敲除的PDAC细胞中,再次验证表明COX2表达水平明显降低。不仅如此,如果回补野生型GOT2,或是加装核定位信号肽的 加强版 GOT2,都能够恢复PPAR 转录活性和COX2的表达水平,并令GOT2敲除PDAC肿瘤组织中浸润T细胞数量再降低,ARG+的巨噬细胞比例也回复到对照组水平。
这些说明,GOT2确实通过提高PPAR 转录活性来影响肿瘤生长的免疫环境,且COX2起到关键作用。
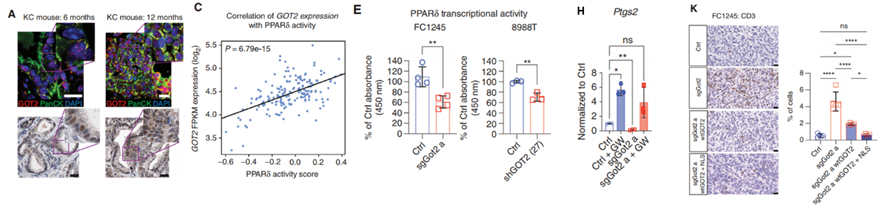
GOT2提高PPAR 转录活性
为了弄清GOT2是如何与脂肪酸联系起来,研究人员解析出GOT2的蛋白结构,并锁定了5个会和脂肪酸结合的疏水区域。其中在2号区域还会更偏爱与PPAR 的重要配体花生四烯酸结合,并且不同种属之间高度保守。当研究人员选择突变该区域内几个核心位点后,这种突变型GOT2的核定位能力、脂肪酸结合能力以及对PPAR 转录调控作用均会明显被抑制。
此外,研究人员在已敲除GOT2的PDAC小鼠模型中回补野生型的GOT2能够完全挽回肿瘤生长的劣势,并且能够抵消GOT2敲减对肿瘤生长、T细胞浸润的作用。但如果回补的是脂肪酸结合位点发生突变的GOT2,却只能恢复部分肿瘤生长优势,对T细胞和ARG+巨噬细胞浸润也只产生较弱的影响,说明2号区域正是GOT2影响肿瘤生长免疫环境的核心区域。
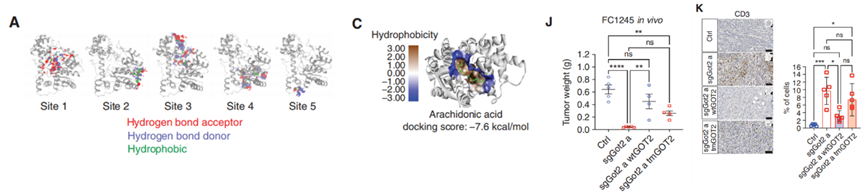
GOT2与PPAR 配体直接结合
基于上述结果,研究人员认为GOT2-PPAR 间的信号传递是影响PDAC瘤内免疫环境和影响肿瘤进展的关键。于是研究人员在GOT2敲除组小鼠中,给予PPAR 激活的药物或病毒诱导处理,并进行观察。实验结果显示,将GOT2敲除后再次激活PPAR 转录功能,依旧可以重拾免疫抑制作用,并且恢复肿瘤的生长优势。
为了进一步弄清GOT2-PPAR 信号通路具体通过哪些基因影响了免疫,研究人员还使用RNA-Seq筛选出PPAR 激动剂处理组和敲除GOT2组间的差异基因,发现其中许多有涉及到免疫细胞趋化和调控免疫功能的关键基因。
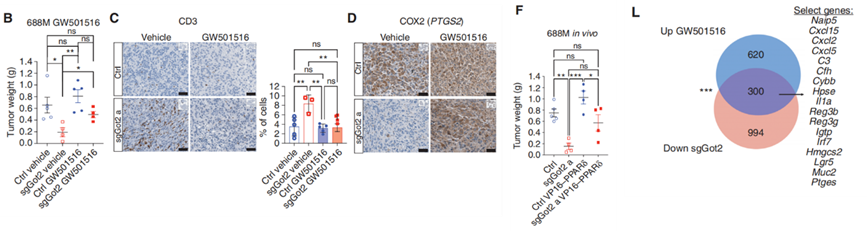
激活PPAR 可抵消GOT2敲减对肿瘤生长和T细胞耗竭的影响
综上,该团队的研究工作揭示了代谢酶GOT2的非经典非代谢功能,证明GOT2还可以通过结合核内脂肪酸配体调控PPAR 转录活性,从而干预免疫相关基因表达并对肿瘤生长免疫环境产生影响。
参考文献:
[1] Xu D, Shao F, Bian X, Meng Y, Liang T, Lu Z. The Evolving Landscape of Noncanonical Functions of Metabolic Enzymes in Cancer and Other Pathologies. Cell Metab. 2021;33(1):33-50. doi:10.1016/j.cmet.2020.12.015.
[2] Abrego J, Sanford-Crane H, Oon C, et al. A cancer cell-intrinsic GOT2-PPARd axis suppresses antitumor immunity [published online ahead of print, 2022 Jul 27]. Cancer Discov. 2022;CD-22-0661. doi:10.1158/2159-8290.CD-22-0661.
[3] Yang H, Zhou L, Shi Q, et al. SIRT3-dependent GOT2 acetylation status affects the malate-aspartate NADH shuttle activity and pancreatic tumor growth. EMBO J. 2015;34(8):1110-1125. doi:10.15252/embj.201591041.
[4] Stump DD, Zhou SL, Berk PD. Comparison of plasma membrane FABP and mitochondrial isoform of aspartate aminotransferase from rat liver. Am J Physiol. 1993;265(5 Pt 1):G894-G902. doi:10.1152/ajpgi.1993.265.5.G894.
[5] Auciello FR, Bulusu V, Oon C, et al. A Stromal Lysolipid-Autotaxin Signaling Axis Promotes Pancreatic Tumor Progression. Cancer Discov. 2019;9(5):617-627. doi:10.1158/2159-8290.CD-18-1212.
[6] Chakrabarti G, Moore ZR, Luo X, et al. Targeting glutamine metabolism sensitizes pancreatic cancer to PARP-driven metabolic catastrophe induced by -lapachone. Cancer Metab. 2015;3:12. Published 2015 Oct 12. doi:10.1186/s40170-015-0137-1.
这类代谢酶的非经典、非酶功能的相关研究不仅丰富了人们对肿瘤代谢酶的认知,还另辟思路的找到了重塑肿瘤生存环境的新治疗靶点。
在未来,或许对于已知基因非经典功能会有更多新的发现,奇点糕也希望这些基因能够更好的指导药物研发造福临床。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- PNAS:免疫疗法新突破!NOD2基因变异助力癌症治疗 (2025-08-06)
- 《自然· 医学》:按照膳食指南吃可能还不够!最新临床试验显示,即使遵照指南要求吃饭,多吃超加工食品仍会阻碍减重 (2025-08-06)
- 施一公团队发表最新PNAS论文 (2025-08-06)
- 致癌代谢物2HG竟是肥胖“隐形推手”?!Nat Metabol 最新研究中科学家揭秘肥胖发生新机制 (2025-08-05)
- Sci Adv:科学家有望重新训练中性粒细胞来靶向治疗乳腺癌 (2025-08-05)
- 特洛伊木马:复旦大学最新论文登上Cell子刊封面 (2025-08-05)
- TN:南京医科大学团队发现,长期运动可通过改善脑膜淋巴管结构和引流功能,减轻AD病理,并改善小鼠认知功能 (2025-08-05)
- 柳叶刀:塑料危机——对人类从摇篮到坟墓的健康威胁 (2025-08-05)
- Nature子刊:中山大学林浩添/陈崴团队开发AI模型,利用视网膜图像无创诊断慢性肾病 (2025-08-05)
- 四部分脱手!医疗科普不是“流量生意” (2025-08-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















