1型糖尿病(T1D)取得重大进展!FDA批准Tzield:首个可延缓1型糖尿病发病的药物! |
 |
来源:100医疗网原创2022-11-22 10336013
Tzield(替利珠单抗)是第一种可以预防/延缓高危人群临床1型糖尿病(T1D)发展的疗法。2周的疗程将患病风险降低了50%,并将发病时间推迟了25个月(2年)。

2022年11月17日/BION/--PROVENTION BIO是一家致力于拦截和预防介导性疾病的生物制药公司。近日,该公司宣布美国美国食品药品监督管理局()已批准Tzield(teplizumab-mzwv)注射液:该药物为静脉注射用抗CD3单克隆抗体,用于目前患有2期1型(T1D)的成人和儿童患者(8岁)的首个也是唯一的免疫调节治疗,以延迟3期T1D(临床T1D)的发病。在药物治疗方面,Tzield每天静脉输注一次,连续14天。
值得一提的是,Tzield是第一个可以阻止/延缓特定人群发展为临床T1D(3期T1D)的疗法,这是自一个世纪前胰岛素问世以来,T1D治疗的第一个重大进展。来自关键TN-10研究的数据显示,与安慰剂相比,在2期T1D的症状前患者中,单次2周(14天)的Tzield治疗将胰岛素依赖性临床疾病(3期T1D)的中位时间延迟了25个月或约2年(50个月对25个月),这代表了3期T1D发病时间的显著学术延长。
Tzield是T1D的首个疾病纠正疗法。T1D是一种危及生命的自身免疫性疾病。2T1D期定义为存在两种或两种以上T1D相关自身抗体和血糖代谢紊乱。第三阶段T1D的开始是改变人生的时刻。进展到3期T1D的患者最终需要终身注射胰岛素。3T1D阶段与严重的健康风险相关,包括危及生命的糖尿病酮症酸中毒。
Tzield通过优先审查程序获得批准,之前曾获得突破性治疗认证(BTD)。目前,Tzield也正在接受欧洲药品管理局(EMA)的检查。在欧盟,Tzield之前被授予优先药物资格(PRIME)。它是PRIME EMA推出的快速审批项目,类似于美国FDA的BTD项目,旨在加快医疗短缺领域关键药物的审评进程。
FDA药物评估和研究中心糖尿病、脂质紊乱和肥胖部主任约翰夏勒茨(John Sharretts)表示:今天批准的一流疗法为一些高危T1D患者带来了重要的新治疗选择。药物延迟(T1D)的临床诊断潜力可能为患者提供数月至数年的无病负担。
2022年10月,Provention Bio宣布与赛诺菲就在美国上市Tzield达成联合推广协议,以延缓高危人群临床T1D的发病。赛诺菲美国公司全科医学负责人Olivier Bogillot说:这一批准是糖尿病社区一个意义深远、期待已久的胜利。我们赞扬Proventio Bio坚定不移地将首个T1D疾病矫正疗法带给患者。我们期待利用赛诺菲在内分泌学领域建立的基础设施和专业知识,为全美有需要的患者提供服务。
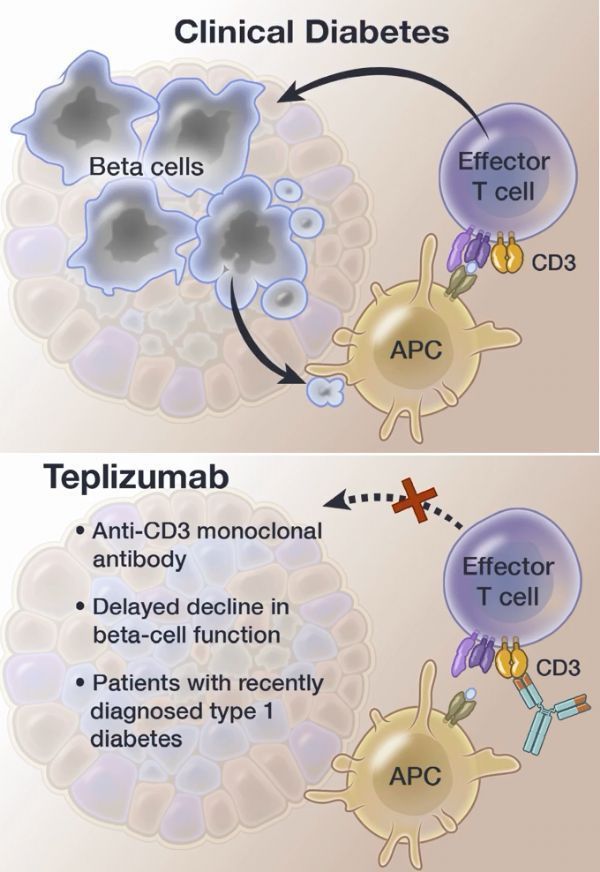
替利珠单抗的作用机制
1型糖尿病(T1D)是一种当免疫系统攻击并破坏产生胰岛素的细胞时发生的疾病。被诊断为T1D的患者血糖升高,需要注射胰岛素(或佩戴胰岛素泵)才能存活,并且必须全天定期检查血糖水平。虽然T1D可以出现在任何年龄,但通常在儿童和年轻人中诊断。虽然大多数T1D患者没有家族史,但如果其父母、兄弟或姐妹患有T1D,则患T1D的风险更高。
Tzield(替普利珠单抗)是一种抗CD3单克隆抗体,用于拦截和预防临床T1D。Tzield与特定的免疫系统细胞结合,并延迟进展到3期T1D。Tzield可以使攻击胰岛素产生细胞的免疫细胞失活,同时增加帮助调节免疫反应的细胞的比例。
Tzield已经在几项临床研究中进行了评估,涉及1000多名患者,其中800多名患者接受了Tzield治疗。先前对新诊断患者的研究表明,替利珠单抗继续证明其维持细胞功能和减少外源性胰岛素使用的能力。
批准基于TrialNet的TN-10研究(有风险,NCT01030861)的临床数据。这是一项关键的随机、双盲、事件驱动、安慰剂对照临床试验,旨在评估替利珠单抗在延迟2期T1D患者3期T1D发作方面的疗效和安全性。结果显示,与安慰剂相比,单次2周(14天)疗程的替利珠单抗治疗显著延迟了高危儿童和成人临床T1D的发病和诊断,T1D的发病率下降了50%,发病的中位时间延迟了25个月或约2年。
这些数据清楚地表明
显示,短期免疫治疗可以显著延缓T1D的临床发生,开发不需要连续治疗以影响自身免疫性疾病的免疫调节药物将是一个重大的模式转变。根据TN-10研究,teplizumab是第一个可显著延迟T1D临床发病的免疫调节剂,有望干预并从根本上改变高危群体的T1D进展。除了评估teplizumab用于T1D患者亲属中具有高风险个体预防T1D的潜力之外,Provention Bio公司也正在评估teplizumab用于新诊断为胰岛素依赖性T1D患者的疗效(III期PROTECT研究)。
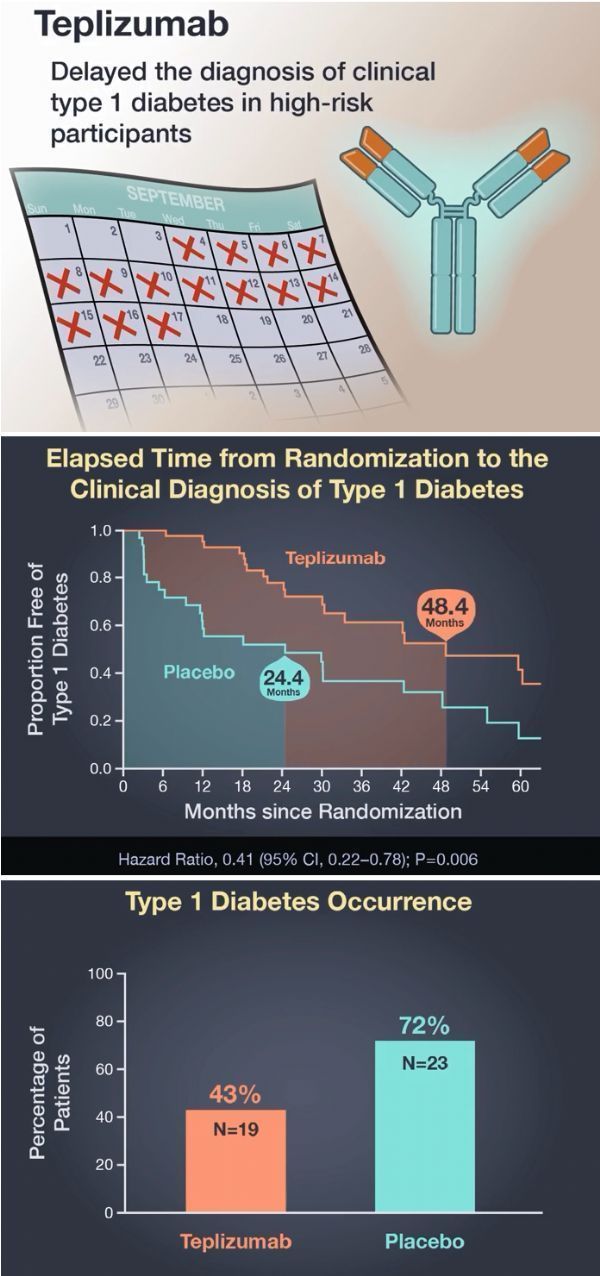
teplizumab临床试验数据(图片来源于:NEJM)
TN-10研究共入组了76例年龄8-49岁的2期T1D受试者,这些受试者是1型糖尿病患者的亲属、存在2种或多种T1D自身抗体和异常的葡萄糖代谢(血糖异常)、没有糖尿病、但有很高的风险发展为糖尿病临床疾病。72%的受试者年龄在18岁以下。研究中,这些受试者随机接受teplizumab或安慰剂治疗。
研究结果已发表于国际医学期刊《新英格兰医学杂志》(NEJM),文章标题为:An Anti-CD3 Antibody, Teplizumab, in Relatives at Risk for Type 1 Diabetes。数据表明,在高危(2期T1D)儿童和成人中,与安慰剂相比,单个14天疗程teplizumab治疗显著延迟了临床T1D(3期T1D)的发病和诊断,延迟的中位时间为2年。具体为,安慰剂组受试者临床诊断T1D的中位时间为25个月,相比之下,teplizumab组受试者临床诊断T1D的中位时间为50个月(HR=0.41;95%CI:0.22-0.78;p=0.0066)。在研究期间,安慰剂组有72%的患者出现临床糖尿病,teplizumab组仅为45%。研究中,teplizumab的耐受性良好,安全性数据与先前对新诊患者的研究一致。
这项具有里程碑意义的突破性研究表明,可以使用免疫疗法,特别是teplizumab,来预防或显著延缓临床1型糖尿病发作至少2年时间。更重要的是,研究中约60%的受试者在一个疗程的teplizumab治疗后没有出现T1D,比例是安慰剂组的2倍。
teplizumab是第一个显示可延迟T1D临床发病的免疫调节剂。其临床结果对于有患1型糖尿病风险的个人,如患者家属,具有真正的临床意义。延迟临床T1D的发病可能意味着疾病负担可能会推迟到患者能够更好地管理其疾病的时间,例如婴儿期、小学、高中甚至大学之后。teplizumab上市后,临床医生将可以干预并从根本上改变这些高危受试者的T1D进展。(100医药网100yiyao.com)
原文出处:
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- PNAS:免疫疗法新突破!NOD2基因变异助力癌症治疗 (2025-08-06)
- 《自然· 医学》:按照膳食指南吃可能还不够!最新临床试验显示,即使遵照指南要求吃饭,多吃超加工食品仍会阻碍减重 (2025-08-06)
- 施一公团队发表最新PNAS论文 (2025-08-06)
- 致癌代谢物2HG竟是肥胖“隐形推手”?!Nat Metabol 最新研究中科学家揭秘肥胖发生新机制 (2025-08-05)
- Sci Adv:科学家有望重新训练中性粒细胞来靶向治疗乳腺癌 (2025-08-05)
- 特洛伊木马:复旦大学最新论文登上Cell子刊封面 (2025-08-05)
- TN:南京医科大学团队发现,长期运动可通过改善脑膜淋巴管结构和引流功能,减轻AD病理,并改善小鼠认知功能 (2025-08-05)
- 柳叶刀:塑料危机——对人类从摇篮到坟墓的健康威胁 (2025-08-05)
- Nature子刊:中山大学林浩添/陈崴团队开发AI模型,利用视网膜图像无创诊断慢性肾病 (2025-08-05)
- 四部分脱手!医疗科普不是“流量生意” (2025-08-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















