豪森获得13个首仿 6个新药 29个一类新药脱颖而出 |
 |
近日,浩森药业产品线迎来新年又有进展:重磅双抗大规模推出,一类新药HS-10390片首次临床申报...............仿制药方面,2017年以来,公司已批准13个首仿(含剂型首仿)。此外,还有10个新的分类产品正在审查中,其中6个暂时没有批准。
拿下13个首仿、6款新药,5个品种闯关新医保
2022年,全民医保谈判在即。根据前段时间公布的初审名单,豪森药业有5个目录外品种,均为2017年1月1日至2022年6月30日期间国家药品监督管理局批准上市的新仿制药。
据我网数据显示,2017年以来,豪森药业已有30多个品种获批上市,其中6个为新药(4个一类新药、1个进口新药、1个改良新药)。目前公司已批准7个新药(5个一类新药)上市。得益于创新药的相继获批和商业化,豪森药业创新药收入从2020H1的7.5亿元增长到2022H1的23.2亿元,创新药收入占总收入的比重从2020H1的18.9%增长到2022H1的52.3%。
此外,13个为首次仿制(包括剂型首次仿制),涵盖8个治疗类别,其中消化代谢类药物5个,抗肿瘤和免疫调节剂3个。目前公司仍有10个新分类产品在审,其中6个未通过首次审批。
2017年起,豪森药业获批上市新药及其首仿品。
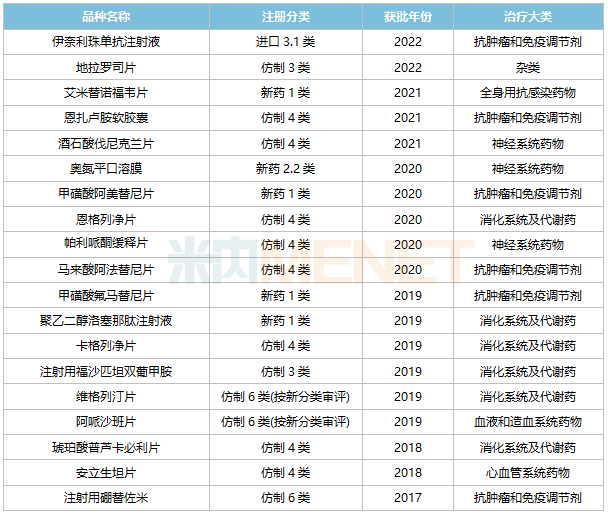
来源:Minenet中国申报进展(MED)数据库
豪森药业上市的6个独家创新药中,已有5个通过谈判纳入国家医保目录,其中甲磺酸阿米替尼片新适应症有望参与2022年医保谈判;2022年获批上市的伊那里珠单抗注射液(国内首个抗CD19单克隆抗体)已通过形式审查,2022年有望通过谈判纳入医保。
近三年达成10余项合作,引进多款差异化新药
11月14日,豪森药业发布公告称,公司与普米思签署许可协议,将获得大中华区(包括中国大陆、香港、澳门和台湾省)PM1080的独家开发和商业化权利,并向普米思支付5000万元首付款、基于销售额的开发、注册和商业化里程碑潜在付款14.18亿元,以及基于净销售额的分级特许权使用费。
PM1080是一种EGFR/c-Met双特异性抗体药物,具有同时阻断EGFR和c-Met信号转导,抑制肿瘤生长和存活的巨大治疗潜力。目前EGFR/c-Met双抗体在国内还没有获批上市,PM1080处于临床前研究阶段。
近年来,浩森药业不断加大对外合作,拓宽产品管道,2020年至今已达成10余笔BD交易。合作企业有普米思、倪康、蒂温比奥、GHDDI、燕鸥、Scynexis、沉默、知道生物、王石智慧等。其中静默交易总额最高超过13亿美元。
2020年以来,豪森药业公司引进的一些项目陆续引进。
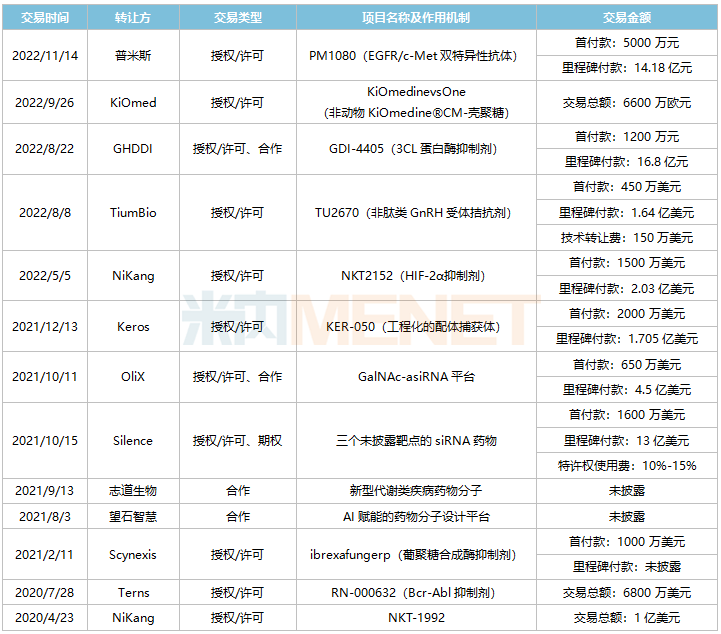
来源:公司公告,迷你网整理
从豪森药业近几年引进的项目来看,主要分为三种:一是临床后期的成熟创新产品,如抗真菌新药ibrexafungerp,2021年在美国获批上市,目前在国内进行三期临床;二是引入早期产品,丰富管道储备,如从沉默引入的三种siRNA药物;三是引进全球先进的技术平台,如AI使能的药物分子设计平台、GalNAc-asiRNA平台等。
从引进新药的研发进展来看,伊布沙芬格普(右旋糖酐)
成酶抑制剂)外阴阴道念珠菌病适应症已在国内开展III期临床;RN-000632(Bcr-Abl抑制剂)慢性髓性白血病适应症在国内开展I期临床;KER-050、NKT2152、TU2670全球最高研发进展均步入II期临床,国内暂未申报临床。
33款新药在路上,第6款1类新药上市在即
除了积极探索可能的BD合作,豪森药业也在不断加码自主研发。半年业绩报告显示,2022H1公司研发开支7.39亿元,同比增长7.6%,占营收比重16.7%(2021年同期为15.6%)。
2020-2022年同期豪森药业研发开支情况(单位:万元)
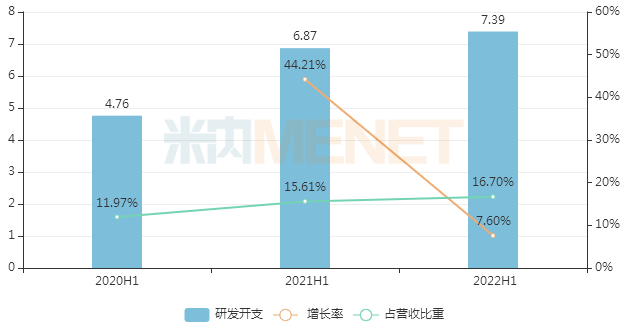
来源:公司公告
米内网数据显示,目前豪森药业有33款创新药处于申报临床及以上阶段(不含已上市新药申报新适应症),涵盖抗肿瘤、神经系统、抗感染、消化道、心血管等治疗领域,其中29款为1类新药。
豪森药业国内在研新药
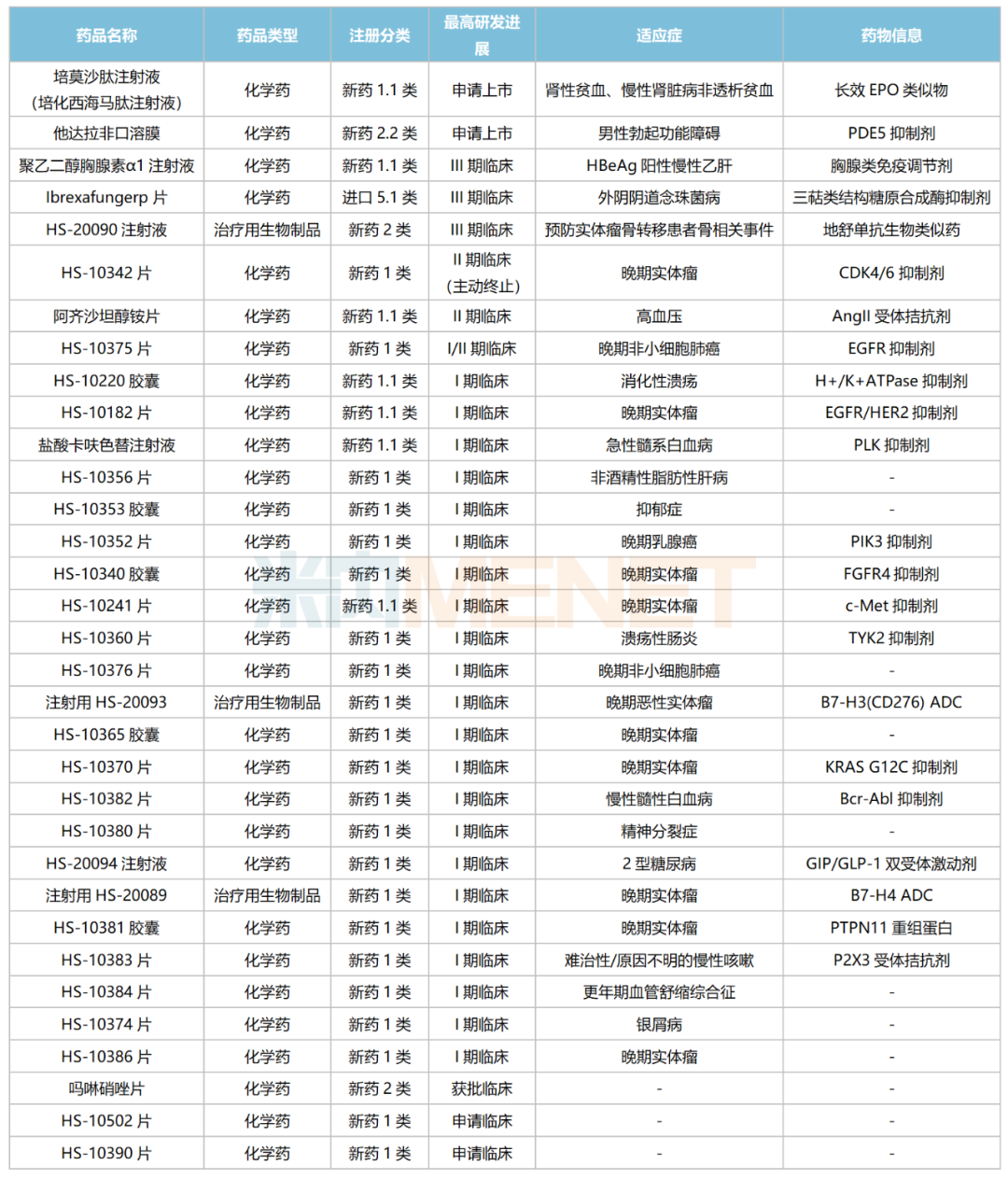
来源:米内网中国临床试验库、CDE官网
29款1类新药中有27款为化学药,涉及CDK4/6、EGFR、PIK3、c-Met等热门靶点。
第6款1类新药——培莫沙肽注射液有望于年内获批上市,目前国内已上市EPO药物以短效为主,尚无国产长效EPO药物获批。米内网数据显示,2021年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端人促红素/重组人促红素销售规模超过35亿元。
豪森药业布局的生物药1类新药不多,但集中在ADC高潜力赛道,靶向B7-H3(CD276)的ADC药物HS-20093、靶向B7-H4的ADC药物HS-20089均在开展实体瘤适应症的I期临床。
非1类新药紧盯高端制剂及生物类似药。他达拉非口溶膜为公司报产的第2款口溶膜,首款口溶膜——奥氮平口溶膜已于2020年获批;HS-20090注射液为地舒单抗生物类似药,目前正在开展III期临床,安进的地舒单抗2021年全球销售额超过50亿美元。
资料来源:米内网数据库、公司公告等
注:米内网《中国公立医疗机构药品终端竞争格局》,统计范围是:中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院,不含民营医院、私人诊所、村卫生室;上述销售额以产品在终端的平均零售价计算。数据统计截至11月18日,如有疏漏,欢迎指正!
医药网新闻
- 相关报道
-
- PNAS:免疫疗法新突破!NOD2基因变异助力癌症治疗 (2025-08-06)
- 《自然· 医学》:按照膳食指南吃可能还不够!最新临床试验显示,即使遵照指南要求吃饭,多吃超加工食品仍会阻碍减重 (2025-08-06)
- 施一公团队发表最新PNAS论文 (2025-08-06)
- 致癌代谢物2HG竟是肥胖“隐形推手”?!Nat Metabol 最新研究中科学家揭秘肥胖发生新机制 (2025-08-05)
- Sci Adv:科学家有望重新训练中性粒细胞来靶向治疗乳腺癌 (2025-08-05)
- 特洛伊木马:复旦大学最新论文登上Cell子刊封面 (2025-08-05)
- TN:南京医科大学团队发现,长期运动可通过改善脑膜淋巴管结构和引流功能,减轻AD病理,并改善小鼠认知功能 (2025-08-05)
- 柳叶刀:塑料危机——对人类从摇篮到坟墓的健康威胁 (2025-08-05)
- Nature子刊:中山大学林浩添/陈崴团队开发AI模型,利用视网膜图像无创诊断慢性肾病 (2025-08-05)
- 四部分脱手!医疗科普不是“流量生意” (2025-08-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















