《细胞·干细胞》:MSKCC团队发现,与癌症密切相关的拟素化通路,是治疗阿尔茨海默病的潜在新靶点! |
 |
《细胞·干细胞》:MSKCC团队发现,与癌症密切相关的拟素化通路,是治疗阿尔茨海默病的潜在新靶点!
来源:奇点糕 2024-07-07 09:57
这项研究鉴定出了拟素化通路作为神经元年龄相关调节因子,并且在构建基于hPSC的AD疾病模型时,可用于诱导神经元衰老,增强AD表型,不仅为AD提供了新的潜在治疗靶点,也对疾病的体外建模具有重要意义。衰老是(AD)最大的风险因素,即使是出生起就存在 -淀粉样前体蛋白(APP)加工异常的家族性AD 常染色体显性AD(ADAD)患者,也是在中年时期才开始出现神经元丢失和认知。从机制上来说,我们还不了解衰老是如何促进AD发生与进展的。
反之,这一点也为AD的研究造成了干扰。在进行基于人多能(hPSC)的疾病建模时,研究人员通常会对患者来源的成纤维细胞直接重编程,得到衍生的神经元,虽然能够保留衰老特征,但这是否能够很好地代表衰老神经元和识别细胞年龄变化的确定性影响,仍然是个挑战。
为了了解衰老促进AD的机制,斯隆-凯特琳癌症研究所干细胞生物学中心的研究团队开展了一项研究,他们揭示了,拟素化(neddylation)通路调节神经元年龄和AD神经退行性病变,在hPSC疾病模型中,诱导细胞衰老有助于增强AD表型。研究结果发表在《细胞 干细胞》杂志上。
这项研究识别出了一种新的AD治疗的潜在靶点,并描述了一种将年龄相关表型编入干细胞疾病模型的策略。
为了确定调节神经元衰老的候选基因,研究人员开发了一个CRISPR全基因组筛选平台,对AD依赖性神经元死亡相关基因进行了筛选。他们构建了一种AD小鼠模型,敲入APPSWE/SWE突变,这种小鼠的总 -淀粉样蛋白(A )是同基因的野生型对照神经元的3倍多,但A 40/A 42比值没有变化。
在野生型和APPSWE/SWE神经元中,研究人员区分了三种不同类别的基因:必需基因、存活或增殖相关基因和 hit 基因,他们要找的hit基因就是AD特异性细胞活性基因。
初筛与二次验证显示,DNAJB11、CEP170B、FAM76B、PPP1CB、VPS36和UBA3的功能缺失与APPSWE/SWE神经元活性明显下降有关,其中DNAJB11、UBA3、VPS36和PPP1CB在老年人皮层中有显著减少。
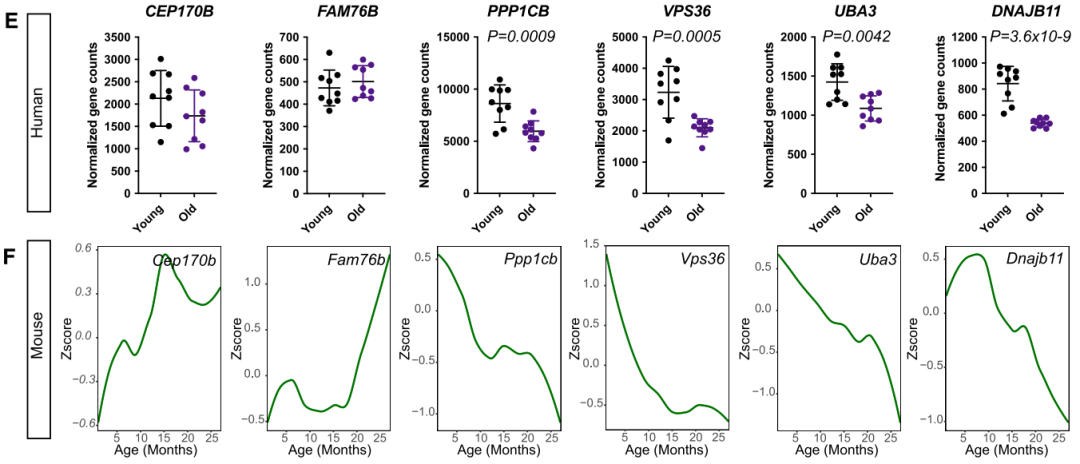
几个hit基因在衰老的人类(E)和小鼠(F)中的减少情况
这些基因中,UBA3引起了研究人员的注意,因为它不属于其他神经元必需性筛选中的必需基因,但在许多分裂细胞(包括系)中是必需的,表明它可能具有神经元特异性作用。
UBA3是用于拟素化(一种类泛素化蛋白质修饰)的二聚体E1连接酶的一个亚基,并且催化拟素化通路的NEDD8激活酶1(NAE1)在筛选中也是一个重要的hit基因,最后,拟素化抑制剂MLN4924已作为癌症候选药物在开发中,它能够诱导DNA损伤和细胞衰老,这也是细胞年龄增加相关表型。
使用MLN4924让拟素化通路失活后,APPSWE/SWE神经元相比野生型表现出更明显的AD相关神经元活性丧失和衰老特征,包括细胞核形态的变化、蛋白质稳态受损(蛋白质错误折叠和聚集)、蛋白酶体功能下降、异染色质丢失和DNA损伤增加。
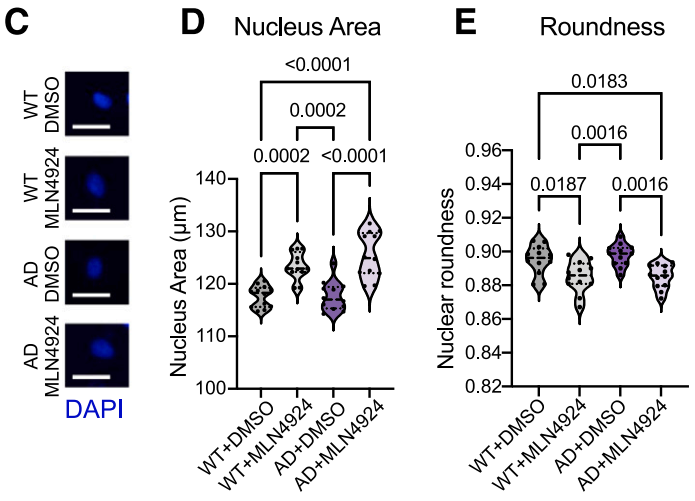
AD和野生型神经元的细胞核形态比较
不但如此,拟素化通路失活还增强了AD特异性tau病理。高分子量磷酸化tau(>250 kDa,HMW pTau)能够促进tau聚集,主要类型的pTau(55kDa,MAJ pTau)减少和HMW pTau增加与tau缠结有关。研究人员发现,拟素化通路失活后,APPSWE/SWE神经元中,MAJ pTau/总tau比值下降,HMW pTau/总tau比值增加,与此前的发现相一致。
去除MLN4924让拟素化通路恢复功能后,神经元的衰老特征得到了逆转。由此,研究人员想到,在神经元还年轻时激活拟素化通路是否能够预防AD的神经退行性病变呢?
于是他们尝试过表达E1连接酶,阻断NEDD8的清除,或者敲除去拟素化酶SENP8,然而,结果与他们的想法完全背道而驰,这些操作加速了A 42诱导的神经元丢失。尽管违背直觉,但抑制去拟素化和抑制拟素化可能具有相同的功能,使得他们构思的 预防措施 无法成立。
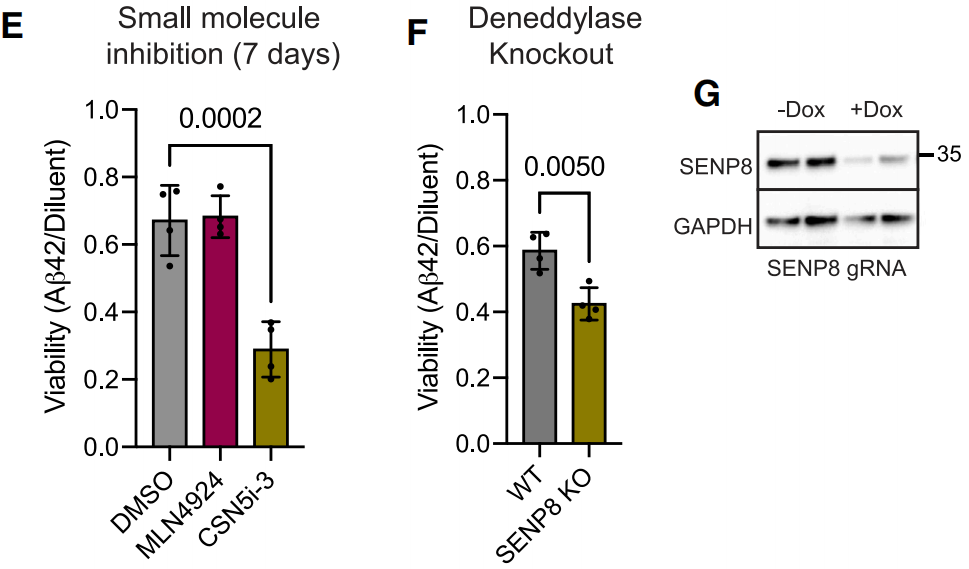
抑制去拟素化加速了神经元丢失
最后,研究人员尝试构建了具有不同遗传风险基因的年龄相关神经退行性疾病的神经元模型,除了APPSWE/SWE和异常A 42神经元外,在另一种AD风险突变PSENM146V/M146V神经元和相关LRRK2G2019S/G2019S多巴胺能神经元中,拟素化通路失活也增加了神经元丢失和神经元活性丧失。
综上所述,这项研究鉴定出了拟素化通路作为神经元年龄相关调节因子,并且在构建基于hPSC的AD疾病模型时,可用于诱导神经元衰老,增强AD表型,不仅为AD提供了新的潜在治疗靶点,也对疾病的体外建模具有重要意义。
衰老是阿尔茨海默病(AD)最大的风险因素,即使是出生起就存在 -淀粉样前体蛋白(APP)加工异常的家族性AD 常染色体显性AD(ADAD)患者,也是在中年时期才开始出现神经元丢失和认知功能障碍。从机制上来说,我们还不了解衰老是如何促进AD发生与进展的。
反之,这一点也为AD的研究造成了干扰。在进行基于人多能干细胞(hPSC)的疾病建模时,研究人员通常会对患者来源的成纤维细胞直接重编程,得到衍生的神经元,虽然能够保留衰老特征,但这是否能够很好地代表衰老神经元和识别细胞年龄变化的确定性影响,仍然是个挑战。
为了了解衰老促进AD的机制,斯隆-凯特琳癌症研究所干细胞生物学中心的研究团队开展了一项研究,他们揭示了,拟素化(neddylation)通路调节神经元年龄和AD神经退行性病变,在hPSC疾病模型中,诱导细胞衰老有助于增强AD表型。研究结果发表在《细胞 干细胞》杂志上[1]。
这项研究识别出了一种新的AD治疗的潜在靶点,并描述了一种将年龄相关表型编入干细胞疾病模型的策略。
为了确定调节神经元衰老的候选基因,研究人员开发了一个CRISPR全基因组筛选平台,对AD依赖性神经元死亡相关基因进行了筛选。他们构建了一种AD小鼠模型,敲入APPSWE/SWE突变,这种小鼠的总 -淀粉样蛋白(A )是同基因的野生型对照神经元的3倍多,但A 40/A 42比值没有变化。
在野生型和APPSWE/SWE神经元中,研究人员区分了三种不同类别的基因:必需基因、存活或增殖相关基因和 hit 基因,他们要找的hit基因就是AD特异性细胞活性基因。
初筛与二次验证显示,DNAJB11、CEP170B、FAM76B、PPP1CB、VPS36和UBA3的功能缺失与APPSWE/SWE神经元活性明显下降有关,其中DNAJB11、UBA3、VPS36和PPP1CB在老年人皮层中有显著减少。
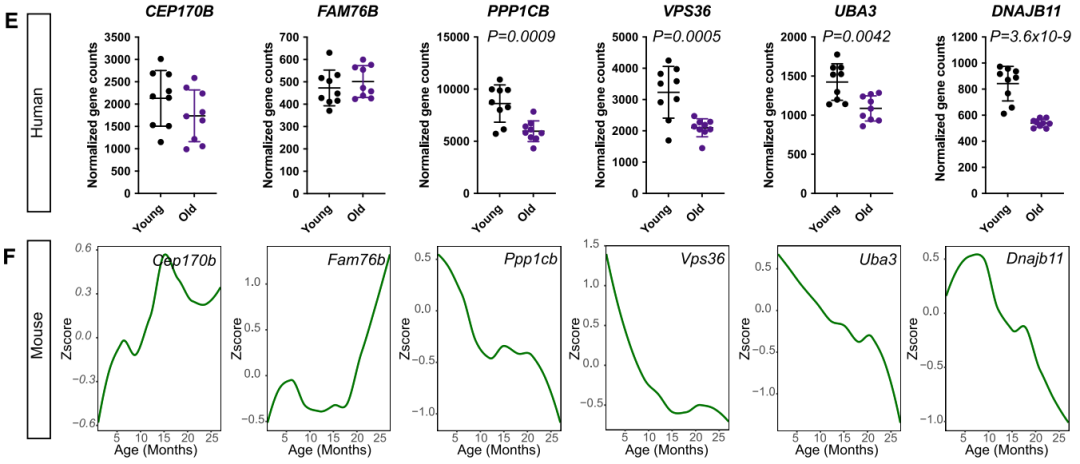
几个hit基因在衰老的人类(E)和小鼠(F)中的减少情况
这些基因中,UBA3引起了研究人员的注意,因为它不属于其他神经元必需性筛选中的必需基因,但在许多分裂细胞(包括癌细胞系)中是必需的,表明它可能具有神经元特异性作用。
UBA3是用于拟素化(一种类泛素化蛋白质修饰)的二聚体E1连接酶的一个亚基,并且催化拟素化通路的NEDD8激活酶1(NAE1)在筛选中也是一个重要的hit基因,最后,拟素化抑制剂MLN4924已作为癌症候选药物在开发中,它能够诱导DNA损伤和细胞衰老,这也是细胞年龄增加相关表型。
使用MLN4924让拟素化通路失活后,APPSWE/SWE神经元相比野生型表现出更明显的AD相关神经元活性丧失和衰老特征,包括细胞核形态的变化、蛋白质稳态受损(蛋白质错误折叠和聚集)、蛋白酶体功能下降、异染色质丢失和DNA损伤增加。
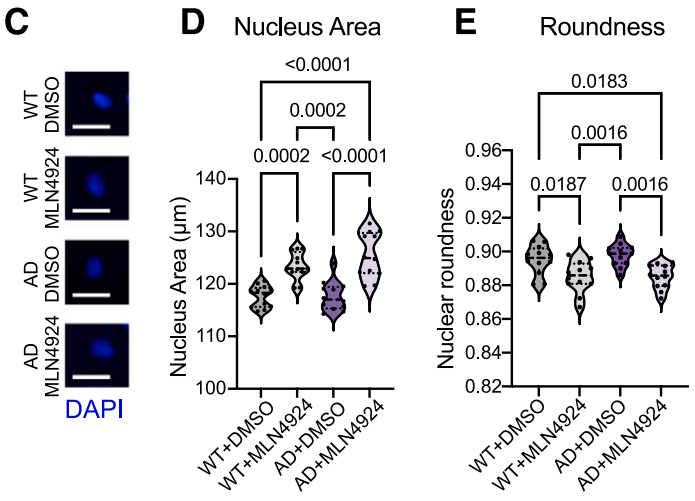
AD和野生型神经元的细胞核形态比较
不但如此,拟素化通路失活还增强了AD特异性tau病理。高分子量磷酸化tau(>250 kDa,HMW pTau)能够促进tau聚集,主要类型的pTau(55kDa,MAJ pTau)减少和HMW pTau增加与tau缠结有关。研究人员发现,拟素化通路失活后,APPSWE/SWE神经元中,MAJ pTau/总tau比值下降,HMW pTau/总tau比值增加,与此前的发现相一致。
去除MLN4924让拟素化通路恢复功能后,神经元的衰老特征得到了逆转。由此,研究人员想到,在神经元还年轻时激活拟素化通路是否能够预防AD的神经退行性病变呢?
于是他们尝试过表达E1连接酶,阻断NEDD8的清除,或者敲除去拟素化酶SENP8,然而,结果与他们的想法完全背道而驰,这些操作加速了A 42诱导的神经元丢失。尽管违背直觉,但,抑制去拟素化和抑制拟素化可能具有相同的功能,使得他们构思的 预防措施 无法成立。
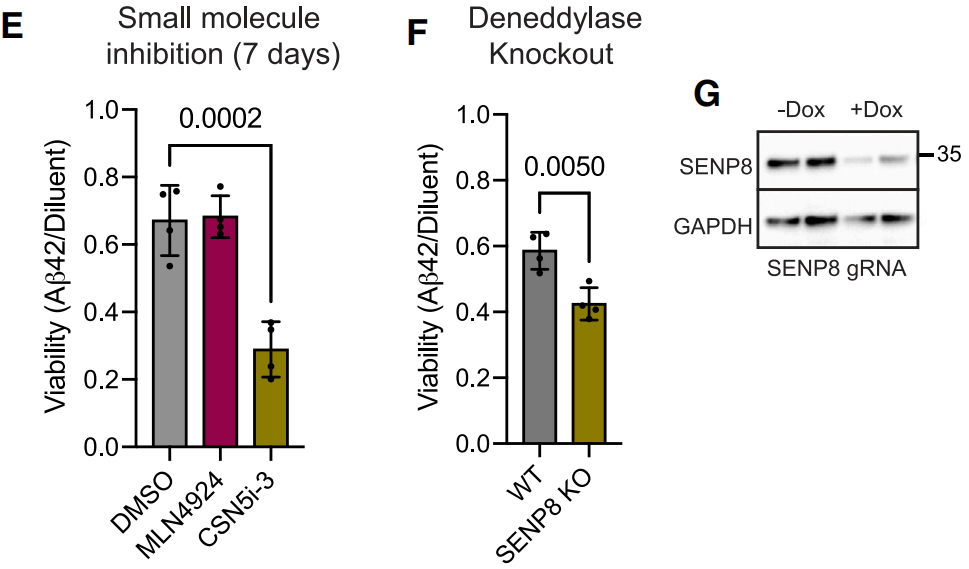
抑制去拟素化加速了神经元丢失
最后,研究人员尝试构建了具有不同遗传风险基因的年龄相关神经退行性疾病的神经元模型,除了APPSWE/SWE和异常A 42神经元外,在另一种AD风险突变PSENM146V/M146V神经元和帕金森病相关LRRK2G2019S/G2019S多巴胺能神经元中,拟素化通路失活也增加了神经元丢失和神经元活性丧失。
综上所述,这项研究鉴定出了拟素化通路作为神经元年龄相关调节因子,并且在构建基于hPSC的AD疾病模型时,可用于诱导神经元衰老,增强AD表型,不仅为AD提供了新的潜在治疗靶点,也对疾病的体外建模具有重要意义。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 【9月23日直播预告】非靶代谢流线上分享会——解码代谢动态,探寻疾病机制 (2025-09-19)
- 【参会指南】9月26-27日,2025(第九届)细胞外囊泡前沿与转化大会(厦门站)即将开幕! (2025-09-18)
- 西湖大学最新Cell子刊论文:利用孕妇肠道菌群预测早产风险 (2025-09-17)
- Cell:高分子量tau蛋白抑制海马体神经元活动,导致阿尔茨海默病的认知衰退 (2025-09-17)
- 两篇《自然》:肺癌私联神经元!科学家首次发现小细胞肺癌细胞会在脑内与神经元形成突触,借助电信号促进肿瘤生长 (2025-09-16)
- Sci Adv:新型双特异性抗体有望成为抗击巨细胞病毒的“免疫特种兵” (2025-09-16)
- 《神经病学》:代糖或伤认知!8年随访发现,摄入较多代糖与记忆力、语言流畅性和整体认知能力下降速度提升32%、173%和62%相关 (2025-09-16)
- Nature子刊:超越ADC,中国博后发明ABC药物,重拳出击,精准靶向 (2025-09-16)
- Cell子刊:“滴血验癌”新突破,王延博/张硕等利用细胞外囊泡,精准检测10多种癌症 (2025-09-16)
- 47亿!派林生物易主中国生物,血液制品行业格局将重塑 (2025-09-15)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















