双剑合璧抗肺癌!浙大团队开发高效低毒肺癌联合疗法 |
 |
【导读】免疫检查点抑制剂(ICIs)免疫疗法在肺癌治疗中已展现出良好的疗效,但 PD-1/PD-L1 抑制剂的整体有效率仅为 20% 至 30%。因此,需要更有效的联合疗法。
7月10日,浙江大学研究人员在期刊《Advanced Science》上发表了研究论文,题为 Targeting Cystine Metabolism in the Lung Cancer Environment Enhances the Efficacy of Immune Checkpoint Inhibition ,本研究发现,肺癌患者肿瘤组织中的胱氨酸和半胱氨酸水平显著高于相邻的非肿瘤组织。胱氨酸缺乏会使巨噬细胞极化为 M1 表型,分泌更多的 TNF- 、CXCL9 和 CXCL10。
然而,采用无胱氨酸饮食仅能轻微降低体内肺癌的发展。进一步的研究表明,胱氨酸剥夺或依拉司汀介导的转运抑制在体外和体内均能增加巨噬细胞中 PD-L1 的表达。将无胱氨酸饮食或 IKE 注射与 PD-L1 抗体治疗相结合,可显著抑制小鼠皮下肿瘤的生长。机制研究表明,胱氨酸缺乏导致的谷胱甘肽耗竭通过减少其谷胱甘肽化激活巨噬细胞中的 NF- B。这种效应可通过补充谷胱甘肽或使用 NF- B 抑制剂来逆转。同时,对免疫治疗反应较好的肺癌患者血清谷胱甘肽水平较低。这些发现表明,靶向胱氨酸代谢结合 PD-L1 抑制是一种有前景的治疗策略。

https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202413084
背景知识
非小细胞肺癌(NSCLC)是肺癌中最常见的组织学亚型,约占所有病例的 80% - 85%。近年来,以 PD-1/PD-L1 抗体为代表的免疫检查点抑制剂(ICIs)在癌症治疗中的迅速发展和应用,使许多晚期 NSCLC 患者实现了长期生存。多项临床研究表明,约 20% 的晚期肺癌患者从 ICI 单药治疗或与化疗联合治疗中获得了长期的临床获益。越来越多的证据表明,肿瘤微环境(TME)的组成对 ICI 治疗的效果有显著影响。除了异质性的肿瘤细胞群,TME 还包括浸润的免疫细胞、血管内皮细胞、成纤维细胞、细胞外基质以及各种分泌因子。因此,深入探索和理解 TME 对肺癌免疫治疗的影响,有助于更精准、更有效地提升免疫治疗效果,改善患者预后。
限制胱氨酸可增强PD-L1阻断的治疗效果
由于限制半胱氨酸的摄入可诱导巨噬细胞出现抗肿瘤表型并表达 PD-L1,研究人员接下来研究了在半胱氨酸供应不足的情况下,PD-L1 阻断是否能取得更好的治疗效果。单独使用 CFD 或抗 PD-L1( PD-L1)治疗仅能轻微抑制肿瘤生长并减轻肿瘤重量,但在 CFD 饮食的小鼠中使用 PD-L1 则能显著减缓肿瘤进展。研究人员还比较了四组小鼠脾脏中 CD4+ T 细胞、CD8+ T 细胞和 NK 细胞的比例,未发现显著差异。研究人员发现, PD-L1 治疗的 CFD 小鼠肿瘤浸润 CD8⁺ T 细胞的百分比显著高于 IgG 治疗的 CFD 小鼠、 PD-L1 治疗的 NCD 小鼠以及 IgG 治疗的 NCD 小鼠,这表明存在明显的协同效应。各组间 CD4⁺ T 细胞、巨噬细胞、树突状细胞、自然杀伤细胞和中性粒细胞的百分比相当。
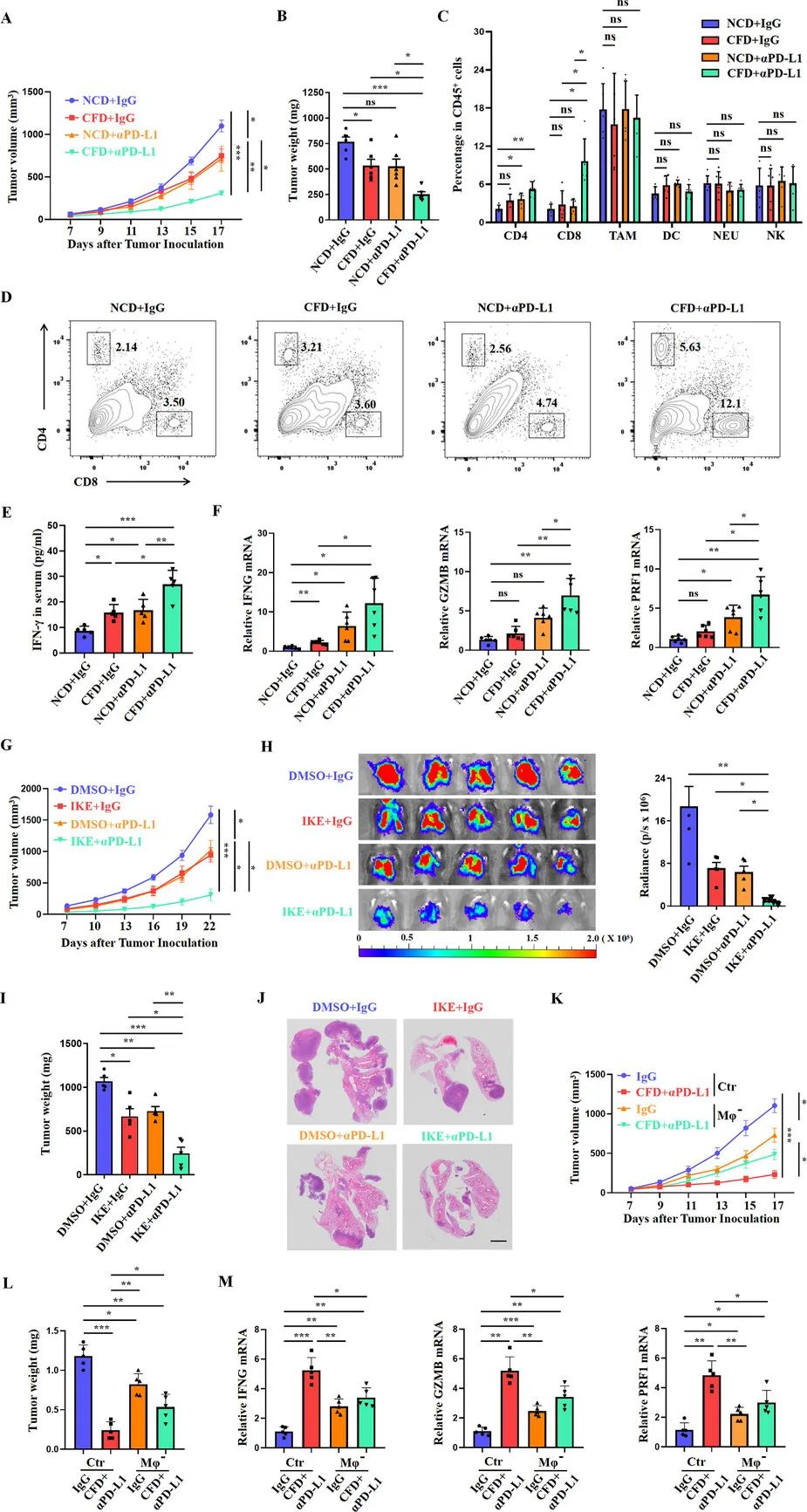
限制半胱氨酸与 PD-L1 抗体疗法协同抑制肺癌进展
为了进一步探究抑制胱氨酸转运是否能使 PD-L1疗法更敏感,研究人员对 LLC 小鼠进行了 IKE、 PD-L1 或两者联合治疗。与对照组和单药治疗组相比,IKE 与 PD-L1 联合治疗显著抑制了肿瘤生长并减轻了肿瘤重量。在 LLC 肿瘤转移模型中,与对照组和单药治疗组相比,用 IKE 加 PD-L1 治疗的小鼠肺部肿瘤负荷显著降低。研究还表明半胱氨酸低微环境对 PD-L1 单克隆抗体的增强作用主要依赖于巨噬细胞。总之,本研究结果表明,低半胱氨酸的肿瘤微环境有利于 PD-L1 阻断疗法发挥最佳疗效,且这种治疗效果依赖于巨噬细胞。
参考资料:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202413084
: , , , , , , , , , , , , 。 视频 小程序 赞 ,轻点两下取消赞 在看 ,轻点两下取消在看 分享 留言 收藏 听过
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 动辄百万美元奖金,这些科学大奖想要与诺贝尔奖竞争:它们含金量如何? (2025-10-06)
- Nature:T细胞耗竭的悖论——并非“精疲力竭”,而是“生产过剩”引发的蛋白毒性风暴 (2025-10-06)
- Cell:沉默的基因组,喧嚣的转录场——解密结核菌适应性的隐藏驱动力 (2025-10-06)
- Nature:谁掌控了人类生命的第一个开关?一个被“驯化”的逆转录病毒的自白 (2025-10-06)
- 三个月,改写生命!全球首例帕金森病实现功能性治愈 (2025-10-05)
- AJP:迄今最长时间真实世界安全性分析显示,艾司氯胺酮鼻喷剂的安全性与临床研究和产品说明书中已确定的一致 (2025-10-05)
- Nature子刊:谭蔚泓/邱丽萍团队开发核酸适配体武装的单核细胞疗法,治疗阿尔茨海默病 (2025-10-05)
- 多学科合作精准拆弹!仁济医院成功救治白塞病合并胸主动脉瘤破裂出血患者 (2025-10-05)
- Nature:自闭症的“双面人生”——迟来的诊断背后,是另一套基因密码吗? (2025-10-05)
- 中国科学院最新论文登上Cell头条 (2025-10-04)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















