Cell:报道循环RNA技术平台以及基于该平台开发的新型抗新冠肺炎疫苗 |
 |
北京大学生命科学学院危文胜课题组
北京大学生命科学学院危文胜研究组在《细胞》杂志上发表了一篇题为《在线》的研究论文,首次报道了环状RNA疫苗的技术平台和抗新冠肺炎的环状RNA疫苗及其一系列变体。在这项研究中,针对新冠肺炎Delta菌株的环状RNA疫苗(circRNARBD-Delta)对多种新冠肺炎菌株具有广谱保护作用。
作为近年来新兴的突破性医学技术,mRNA疫苗的基本原理是通过脂质纳米粒(LNP)将mRNA导入体内表达抗原蛋白,从而刺激机体产生特异性反应。2019年底疫情爆发()后,靶向mRNA疫苗(ModernamRNA-1273;辉瑞/BioNTechBNT162b2)在众多疫苗类型中脱颖而出。mRNA疫苗的修饰和递送技术均由国外机构生产,制约了我国mRNA疫苗及其治疗技术的发展和应用。因此,迫切需要开发新的高效疫苗技术。与线性mRNA不同,环状RNA分子具有共价闭合的环状结构,并且不包含5 -Cap和3 -polyA结构。且稳定性高于未引入修饰碱基的线性RNA。然而,RNA的环化方法和纯化策略尚不成熟,其潜在免疫原性对疫苗开发的影响尚不清楚。许多未知因素制约着环状RNA的发展和应用。
危文胜团队首先建立了体外高效制备高纯度环状RNA的技术平台,并针对新型冠状病毒及其变异体设计了编码新冠肺炎刺突受体结构域(RBD)的环状RNA疫苗。实验证明,该疫苗能在小鼠和恒河猴体内诱导高水平的新冠肺炎中和抗体和特异性T细胞免疫应答,并能有效降低新冠肺炎恒河猴肺部的病毒载量,显著缓解新冠肺炎感染引起的肺炎症状(图2)。
一系列对比评价表明,与mRNA疫苗相比,CircrRNA疫苗具有以下特点或优势(图3): 1 3):1)circRNA具有更高的稳定性,能在体内产生更高水平、更持久的抗原;2) CircrRNA疫苗诱导机体产生更高比例的中和抗体,可以更有效地抵抗病毒变异,降低疫苗的抗体依赖性增强(ADE)的潜在副作用;3)circRNA疫苗诱导的IgG2/IgG1比值较高,表明其主要诱导Th1保护性T细胞免疫应答,可有效降低疫苗相关性增强呼吸道疾病(VAERD)的副作用。
此外,在新冠肺炎的奥密克戎菌株被世界卫生组织列为关注变异体(VOC)后,研究团队紧急启动了针对这种变异体的环状RNA疫苗的研发工作。在获得病毒序列信息的30天内,完成了从疫苗生产、小鼠免疫到效果评价的全过程。发现奥密克戎-based环状RNA疫苗(circrnarbd-omicron)的保护范围较窄,circRNARBD-Omicron诱导的抗体只能中和奥密克戎另一方面,针对Delta株设计的环状RNA疫苗(circRNARBD-Delta)可以在小鼠体内诱导广谱中和抗体,有效中和包括奥密克戎株在内的各种新冠肺炎株(图4)。
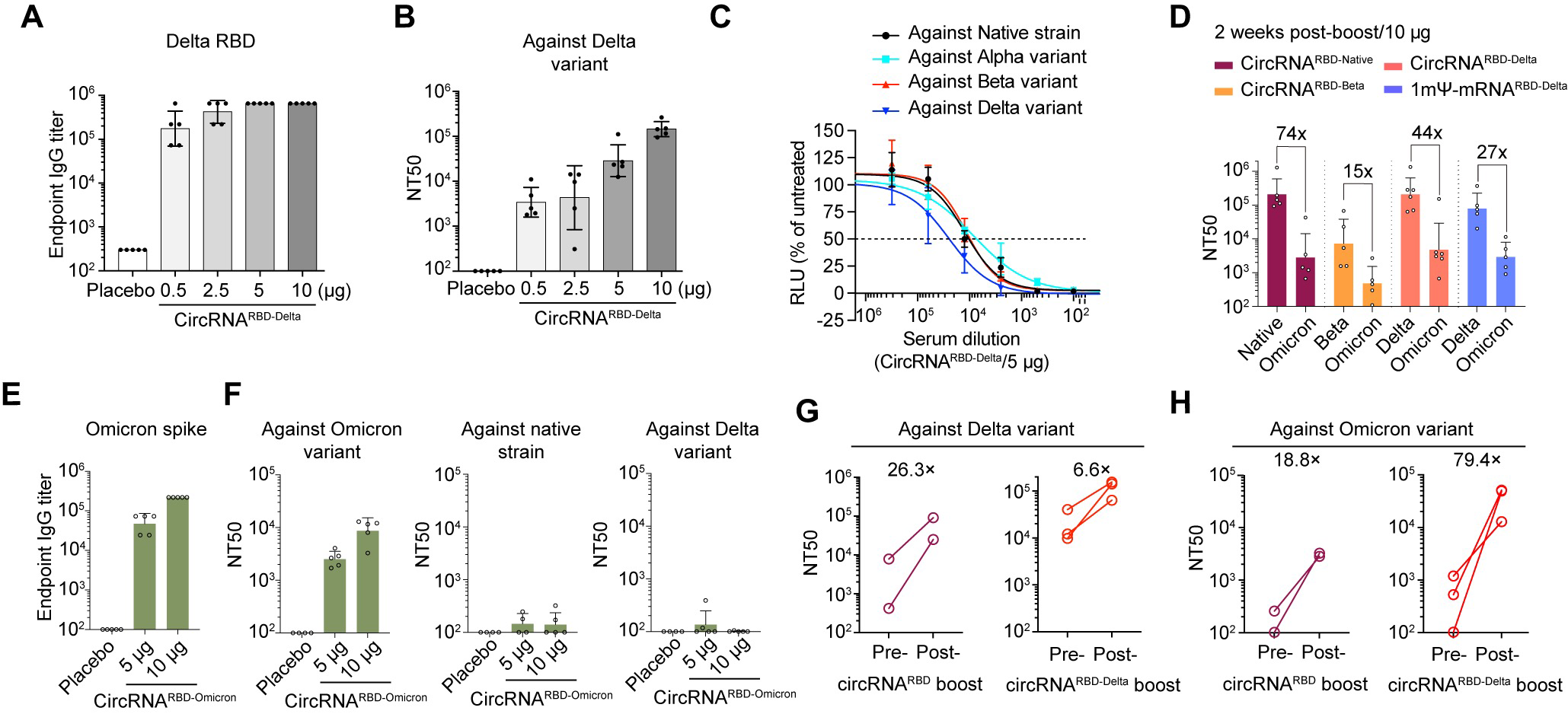
图4针对新冠肺炎Delta株设计的circRNARBD-Delta疫苗是具有广谱保护作用的候选疫苗。
以上结果表明,针对新冠肺炎Delta株设计的circRNARBD-Delta疫苗是一种具有广谱保护作用的新冠肺炎肺炎候选疫苗,本研究也为针对新冠肺炎株快速传播的疫苗研发和疫苗接种策略提供了参考。同时,该平台技术在感染性疾病、自身免疫性疾病、罕见病和癌症的治疗中具有广阔的应用前景。
版权声明
本网站所有标注“来源:100医学网”或“来源:bioon”的文字、图片及音视频资料,版权归100医学网网站所有。未经授权,任何媒体、网站、个人不得转载,否则将追究法律责任。获得书面授权转载时,必须注明“来源:100医学网”。其他来源的文章均为转载文章。本网站所有转载文章都是为了传递更多信息。转载内容不代表本站立场。不想被转载的媒体或个人可以联系我们,我们会立即删除。
87%的用户都在使用100医疗网APP随时阅读、评论、分享、交流。请扫描二维码下载-


- 相关报道
-
- Nature Methods :“垃圾”数据里掘金!流式细胞术迎来革命,解锁百万细胞互作的秘密语言 (2025-08-10)
- Immunity:黄波团队利用生物机械力信号强势扩增干性 CAR-T 细胞,有望颠覆实体肿瘤细胞治疗 (2025-08-10)
- Nature Genetics:大脑里的“冰与火之歌”——揭秘抑郁症中“过热”的神经元与“沉睡”的免疫哨兵 (2025-08-10)
- 《自然·免疫学》:华人科学家首次发现,肿瘤利用激素SCG2调节髓系细胞免疫抑制功能! (2025-08-10)
- Cell:沈西凌团队揭开癌症患者暴瘦的原因,并提出治疗方法 (2025-08-10)
- 今年第5篇Cell、Nature、Science正刊!姜长涛团队最新Cell论文,利用AI工具,挖掘出超60万种胆汁酸代谢酶 (2025-08-09)
- iScience:惊!夜间喝咖啡竟会增加冲动行为,尤其是女性 (2025-08-08)
- 事关脑机接口家当立异倒退 七部分宣布重磅文件 (2025-08-08)
- PD-(L)1/VEGF之后,双抗BD的新王牌藏在哪? (2025-08-08)
- 辉瑞2025H1:ADC产品销售收入15亿美元,还有130亿美元BD弹药 (2025-08-08)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















